Elektronische Konfiguration – das Geheimnis der atomaren Struktur
Im Herbst 1910 Ernest Rutherford, besessen von Gedanken, schmerzlich versucht , die innere zu verstehen Struktur des Atoms. Seine Experimente Dispersion von Alphateilchen diverse Substanzen überzeugend bewiesen – Atom in einem gewissen vorhanden ist, bisher unerforschten, massigen Körper. Im Jahr 1912 nennt es Rutherford würde einen Atomkern. Der Kopf Wissenschaftler schwärmten Tausende von Fragen. Welche Ladung hat diesen unbekannten Körper? Wie hoch ist die Anzahl der Elektronen benötigt um sein Gewicht zu gewährleisten?
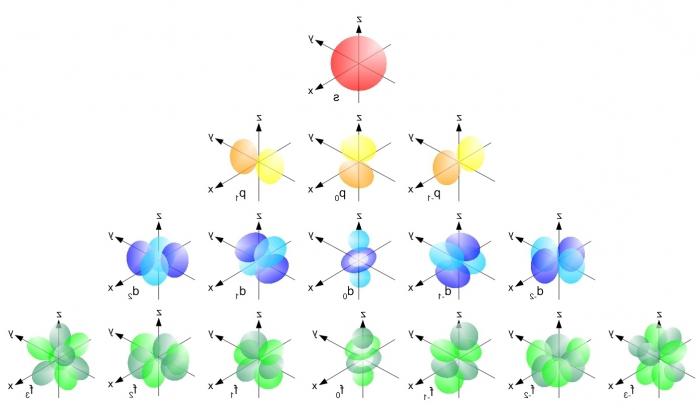
Im Mai 1911 veröffentlichten Rutherford, einen Artikel über die Struktur des Atoms, die eine sehr wichtige Einschränkung geht davon aus, dass die Stabilität der atomaren Struktur ist wahrscheinlich auf den Feinheiten der inneren Struktur des Atoms und die Bewegung von geladenen Teilchen abhängen, die ihre wichtige strukturelle Komponente ist. Kern Elektronen des Atommodells – So wurde die Elektronenkonfiguration geboren. Dieses Modell war dazu bestimmt, eine unschätzbare Rolle in der Kernphysik zu spielen.

Elektronische Konfiguration – ist die Reihenfolge der Verteilung der Elektronen auf Atombahnen. Dank der neugierigen Geist und Ausdauer Ernest Rutherford, die in der Lage war, seine Idee zu verteidigen, Wissenschaft mit neuen Erkenntnissen angereichert wurde, deren Bedeutung kann nicht genug betont werden.
Die elektronische Konfiguration eines Atoms ist. In der Mitte der gesamten Struktur wird für jede Menge von Protonen und Neutronen einen Kern, der aus einem anderen Material angeordnet ist. Und dies ist aufgrund der positiven Ladung des Kerns. Um ihn herum relevante konzentrische Bahnen bewegen sich Elektronen – negativ geladene Elementarteilchen. Diese Atombahnen sind auch Schalen genannt. Die äußere Umlaufbahn des Atoms ist die Valenz genannt. Eine Anzahl von Elektronen auf sie – Wertigkeit.
Jede elektronische Konfiguration der Elemente variiert die Anzahl der Elektronen, die darin enthalten sind. Zum Beispiel kann eine sehr einfache Angelegenheit im Universum – Wasserstoff – mit nur einem einzelnen Elektron, ein Sauerstoffatom, – acht und elektronische Konfiguration Eisen hat sechsundzwanzig Elektronen.
Aber entscheidend für das elektronische Modell des Atoms ist nicht die Anzahl der Elektronen, und was hält sie zusammen und bewirkt, dass das System einwandfrei funktioniert – der Kern und seine Zusammensetzung. Es gibt Substanzkerne individuelle Qualitäten und Eigenschaften. Elektronen verlassen manchmal Atommodell, und dann Atom erwirbt eine positive Ladung (aufgrund der Kernladung). In diesem Fall wird der Stoff nicht seine Eigenschaften ändern. Aber wenn man die Zusammensetzung des Kerns zu ändern, wird es eine ganz andere Sache mit unterschiedlichen Qualitäten. Machen Sie es schwierig, aber immer noch möglich.
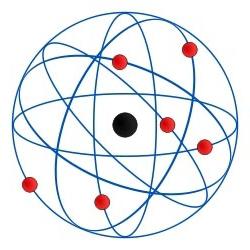
Da die Elektronenkonfiguration nicht möglich, ohne sein Hauptstrukturelement ist – der Atomkern, soll betont werden. Es ist dieses zentrale Element des Atommodell bildet individuellen Eigenschaften und Charakteristiken jeder Chemikalie. Protone, die in der Tat sind, gibt dem Kern eine positive Ladung 1840 mal schwerer als jeder des Elektrons. Aber die Macht der Proton aufladen zu , dass irgendein die Elektronen gleich. Im Zustand des Gleichgewichts der Anzahl der Protonen in einem Atom ist die Anzahl der Elektronen. In diesem Fall ist der Kern der Träger der Null-Ladung.
Ein weiteres großes Teilchen genannt Neutronen des Atomkernes. Es ist dieses Element , das keine Ladung hat, ermöglicht die nukleare Kettenreaktion. So überschätzen den Wert des Neutrons ist einfach unmöglich.