Mikrosomalen Oxidation: Eine Reihe von Reaktionen
Die Rolle der mikrosomalen Oxidation im Leben des Organismus ist schwer zu überschätzen oder übersehen. Die Inaktivierung von xenobiotischen (Giftstoffe), der Zusammenbruch und die Bildung von Nebennieren Hormone beteiligt den Stoffwechsel von Proteinen und Erhaltung der genetischen Information – ist nur ein kleiner Bruchteil der bekannten Probleme werden gelöst durch mikrosomale Oxidation. Es ist ein autonomer Prozess im Körper, die, nachdem sie getroffen von einem Trigger-Substanz und endet mit seinem elliminatsiey ausgeführt wird.
Definition
Mikrosomalen Oxidation – eine Kaskade von Reaktionen, die in der ersten Umsetzungsphase von Xenobiotika. Das Wesen des Verfahrens besteht in der Hydroxylierung von Substanzen mit Sauerstoffatomen und bildet Wasser. Aufgrund der Veränderungen in der Struktur des ursprünglichen Materials und seiner Eigenschaften kann entweder unterdrückt oder verstärkt werden.
Mikrosomalen Oxidation führt Sie in die Konjugationsreaktion. Diese zweite Phase Transformationen von Xenobiotika, dessen Ende eine bestehende funktionelle Gruppe Moleküle innerhalb des Körpers erzeugt angebracht ist. Manchmal Bildung von Zwischenstoffen, die Leberzellschädigung, Nekrose und Gewebedegeneration der Onkologie verursachen.
Oxidation-Oxidase-Typ
Mikrosomalen Oxidationsreaktionen außerhalb der Mitochondrien auftreten und deshalb verbraucht haben etwa zehn Prozent des gesamten Sauerstoff in den Körper eindringen. Schlüsselenzyme in diesem Prozess – Oxidase. In ihrer Struktur sind die Metallatome, die mit variabler Wertigkeit, wie Eisen, Molybdän, Kupfer usw., und daher sind sie in der Lage Elektronen zu akzeptieren. In der Zelle Oxidase aus bestimmten Vesikel (Peroxisomen), die auf den äußeren Membranen der Mitochondrien und in EPR (rauen endoplasmatischen Retikulum). Substrat during Peroxisom verliert Wasserstoffmoleküle, die an gebunden sind , ein Molekül Wasser Peroxid zu bilden.
Es gibt nur fünf Oxidasen:
– monoaminooksigenaza (MAO) – hilft, Adrenalin und andere biogene Amine, die durch die Nebennieren produziert, zu oxidieren;
– diaminooksigenaza (DAO) -, die an der Oxidation von Histamin (Mediator von Entzündungen und Allergien), Polyamine und Diamine;
– L-Aminosäureoxidase (dh linksdrehendes Molekül);
– D-Aminosäureoxidase (rechtsdrehende Moleküle);
– Xanthin – oxidiert Adenin und Guanin (Stickstoffbasen in dem DNA-Moleküle enthalten).
Der Wert der Typ oxidase mikrosomalen Oxidation besteht in der Eliminierung von Xenobiotika und Inaktivierung von biologisch aktiven Substanzen. Bildung Peroxid hat eine bakterizide Wirkung und die mechanische Reinigung des Fehlers ist die Nebenwirkung, die neben anderen Effekten einen wichtigen Platz einnimmt.
Oxidation Oxygenase Typ
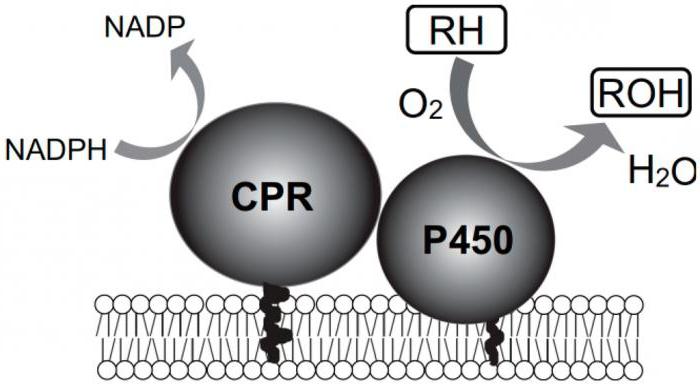
Oxygenase-Reaktion in der Zelle findet auch auf dem rauen endoplasmatischen Retikulum und Mitochondrien-Membranen vneschnih. Dies erfordert eine spezifisches Enzym – Oxygenase, die das Sauerstoffmolekül von dem Substrat zu erhöhen, und es in die oxidierbare Substanz einzuführen. Wenn ein Sauerstoffatom implementiert, das Monooxygenase Enzym oder hydroxylase. Im Fall zwei Atome des Einführens (d.h. eine gesamte Molekül Sauerstoff) wird das Enzym diaksigenaza genannt.
Oxygenase Typ Oxidationsreaktion umfasst einen ternären Multienzymkomplex, der durch die Aktivierung von Sauerstoff in der Übertragung von Elektronen und Protonen vom Substrat gefolgt teilnimmt. Dieser gesamte Prozess erfolgt unter Beteiligung von Cytochrom P450, die noch näher beschrieben werden.
Beispiele Oxygenase Reaktionen
Wie oben erwähnt, für die Oxidation Monooxygenase Verwendung nur eines Sauerstoffatoms der beiden zur Verfügung. Zweitens werden sie an zwei Moleküle Wasserstoff anhaftendes Wasser zu bilden. Ein Beispiel für eine solche Reaktion ist die Bildung von Kollagen. Sauerstoff-Donor wirkt in diesem Fall als Vitamin C. Prolingidroksilaza raubt es von Sauerstoffmolekül und gibt es an Prolin, was wiederum einen Teil des Prokollagen-Moleküls ist. Dieser Prozess gibt die Festigkeit und Elastizität des Bindegewebes. Wenn es ein Mangel an Vitamin C, die Entwicklung von Gicht. Es manifestiert sich die Schwäche des Bindegewebes, Blutungen, blaue Flecken, Verlust der Zähne, das heißt, die Qualität von Kollagen im Körper ist unten.
Ein weiteres Beispiel ist die Hydroxylase, das Cholesterin-Molekül umwandeln. Dies ist eine der Stufen der Bildung von Steroidhormonen, einschließlich Geschlecht ab.
ist nicht spezifisch Hydroxylase
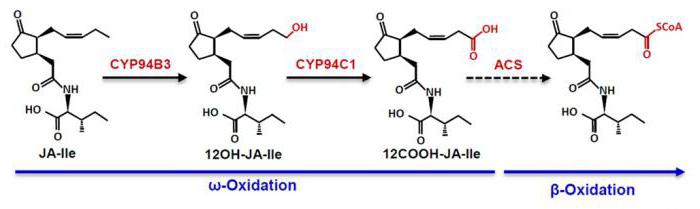
Diese Hydrolase, die für die Oxidation von Fremdstoffen, wie Xenobiotika. Die Bedeutung der Reaktionen ist ein solches Material zugänglicher Entfernung, besser löslich zu machen. Dieser Prozess wird Entgiftung genannt, und es tritt meist in der Leber.
Durch die Verwendung des gesamten Moleküls von Sauerstoff in dem Spalt Xenobiotika Zyklus Reaktionen und Zersetzung des komplexen Stoffes in mehrere einfachere und für metabolische Prozesse erzeugt.
Reaktive Sauerstoffspezies
Sauerstoff ist ein potenziell gefährlicher Stoff, da in der Tat, die Oxidation – ein Verbrennungsprozess. In Form von O 2 -Moleküle oder Wasser ist stabil und chemisch inert, da seine Leistungspegel gefüllt sind und neue Elektronen nicht mitmachen. Jedoch Verbindungen, bei denen der Sauerstoff bei nicht alle ein Elektronenpaar gibt es eine hohe Reaktivität. Deshalb werden sie aktiv genannt.
Solche Sauerstoffverbindungen:
- In monooksidnyh Reaktionen erzeugt Superoxid, die aus dem Cytochrom P450 getrennt ist.
- Die Oxidase-Reaktionen ist die Bildung von Peroxidanion (Wasserstoffperoxid).
- Während der Wiedersauerstoffversorgung des Gewebes, die Ischämie unterzogen wurden.
Das stärkste Oxidationsmittel ist ein Hydroxyl – Radikal, es in einer freien Form existiert nur ein Millionstel einer Sekunde, aber in dieser Zeit Zeit durch eine Reihe von Oxidationsreaktionen zu gehen. Seine Funktion besteht darin, dass das Hydroxylradikal, die Substanz lediglich an dem Ort wirkt, in der gebildet wird, da sie das Gewebe nicht durchdringen können.
Superoxidanion und Wasserstoffperoxid
Diese Substanzen sind aktiv, nicht nur im Bereich der Bildung, sondern auch in einiger Entfernung von ihnen, wie sie durch die Zellmembran durchdringen können.
Hydroxylgruppengehalt bewirkt, dass die Oxidation der Aminosäurereste: Histidin, Cystein und Tryptophan. Dies führt zur Inaktivierung der Enzymsysteme, sowie die Unterbrechung der Transportproteine. Außerdem führt mikrosomalen Oxidation von Aminosäuren zu einer Zerstörung der Struktur von Nukleins stickstoffhaltigen Base, und folglich leidet den genetischen Apparat der Zelle. Und Fettsäuren oxidiert, dass die Zellmembranen bilipidnogo Schicht bilden. Dies wirkt sich auf ihre Durchlässigkeit, Job-Elektrolyt-Membran-Pumpe und die Position des Rezeptors.
Inhibitoren der mikrosomalen Oxidation – sind Antioxidantien. Sie werden in Lebensmitteln gefunden und werden im Körper produziert. Die bekannteste Antioxidans ist Vitamin E. Diese Substanzen mikrosomalen Oxidation hemmen können. Biochemie beschreibt die Wechselwirkung zwischen ihnen auf der Grundlage von Feedback. Das heißt, je mehr Oxidasen, desto mehr werden sie unterdrückt werden, und umgekehrt. Dies trägt dazu bei, ein Gleichgewicht zwischen den Systemen und der Konstanz der inneren Umgebung aufrecht zu erhalten.
Elektrotransportkette
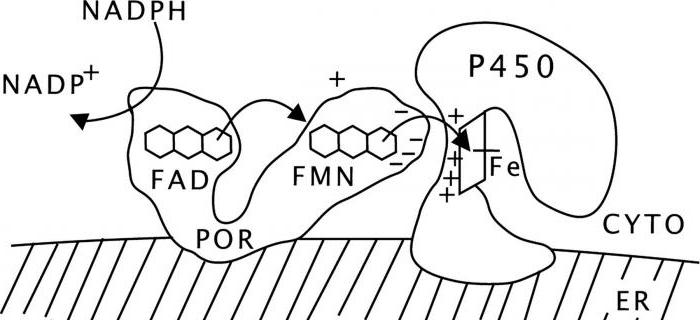
Mikrosomalen Oxidationssystem ist im Cytoplasma der Komponenten nicht löslich sind, so dass alle seine Enzyme auf der Oberfläche des endoplasmatischen Reticulums gesammelt werden. Dieses System enthält mehrere Proteine, die die Elektrotransport-Schaltung bilden:
– NADPH-P450-Reduktase und Cytochrom P450;
– OVER-tsitohromV5-Reduktase und Cytochrom b5;
– steatorrhea-CoA Desaturase.
Der Elektronendonor in der Mehrzahl der Fälle die Handlungen von NADP (Nikotinamidadenindinukleotidphosphat). Es oxidiert NADPH-P450-Reduktase, die zwei Coenzym (FAD und FMN) umfasst, für Elektronen nehmen. Am Ende der Kette FMN oxidierte P450 verwendet wird.
Cytochrom P450
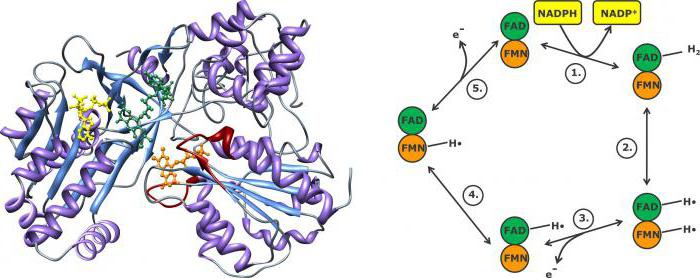
Dieses Enzym der mikrosomalen Oxidation von Häm-enthaltenden Protein. Es bindet Sauerstoff und ein Substrat (in der Regel ein xenobiotic). Sein Name ist mit der Absorption von Licht mit einer Wellenlänge von 450 nm verbunden. Biologen haben es in allen lebenden Organismen entdeckt. Im Moment beschrieben mehr als elftausend Proteine an dem Cytochrom P450-System gehören. Bei Bakterien wird die Substanz im Zytoplasma gelöst, und es wird angenommen, dass diese Form als die von Menschen die evolutionär alten ist. Wir Cytochrom P450 – ein Wandprotein auf der Cytoplasmamembran fixiert.
Die Enzyme dieser Gruppe sind in den Stoffwechsel von Steroiden und Gallen Fettsäuren, Phenolen, Neutralisierungs Drogen, Gifte oder Drogen beteiligt.
Die Eigenschaften von mikrosomalen Oxidations
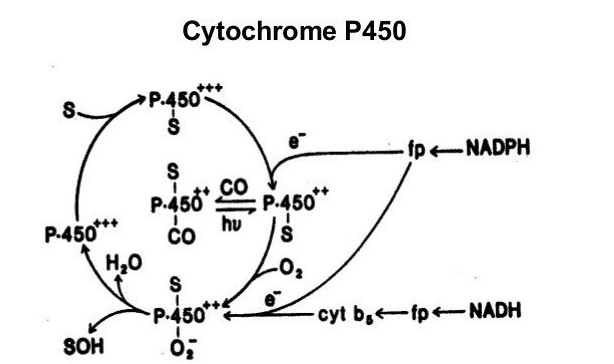
Die Prozesse der mikrosomalen Oxidation haben eine breite Substratspezifität, und dies wiederum ermöglicht eine Vielzahl von Substanzen nachzuweisen. Elftausend Proteine Cytochrom P450 in mehr als einhundertfünfzig Isoformen des Enzyms gefaltet werden. Jeder von ihnen hat eine große Anzahl von Substraten. Dies ermöglicht es dem Körper zu bekommen, fast alle von Schadstoffen zu befreien, die im Inneren gebildet werden oder außerhalb fallen. sowohl in dem Lebermikrosoxidationsenzym Herstellung aus dem Körper am Ort und in einer beträchtlichen Entfernung wirken.
Die Regulation der Aktivität von mikrosomaler Oxidations
Mikrosomalen Oxidation in der Leber auf mRNA-Ebene geregelt, sondern seine Funktion – Transkription. Alle Varianten von Cytochrom P450, zum Beispiel auf dem DNA-Moleküle aufgenommen, und es auf ESR notwendig, um „neu schreiben“, um die Information von der DNA zu Boten-RNA erschien. Dann wird die mRNA-Ribosomen gerichtet, wo die Proteinmoleküle gebildet werden. Die Anzahl dieser Moleküle wird von außen geregelt und ist auf die Menge der Substanzen ab, die abgeschaltet werden müssen, und die Verfügbarkeit von essentiellen Aminosäuren.
Derzeit sind mehr als zweihundertfünfzig beschriebenen chemischen Verbindungen, die den Körper mikrosomalen Oxidation aktivieren. Diese umfassen Barbiturate, aromatische Kohlenwasserstoffe, Alkohole, Ketone und Hormone. Trotz dieser scheinbaren Vielfalt, all diese Substanzen sind lipophile (fettlöslich) und daher anfällig für Cytochrom P450.