Was ist ein Maulwurf in der Chemie? Bestimmung und Formeln
Mit dem Begriff „Maulwurf“ jeden Schülers mit Blick auf die Studie der Chemie beginnt. Bei komplexeren Konzepten wie Molmasse, molaren Konzentration, Molarität Lösungsmittel schwer zu verstehen, nicht was Mol zu kennen. Man erkennt, dass der Maulwurf geschlossen werden – eine der wichtigsten Konzepte in der Chemie. Viele Probleme lassen sich nicht ohne die Bestimmung der Anzahl der Mole gelöst werden.
Definition
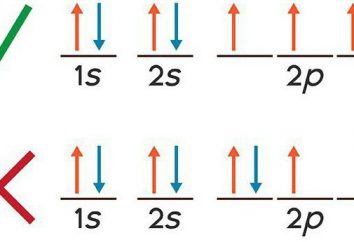
Also, was ist der Maulwurf in der Chemie? Erklärung gibt, ist ganz einfach: es ist eine Einheit, in der die exprimierte Menge des Stoffes eine der SI-Einheiten ist. Bestimmung dessen, was in der Chemie Mol, und kann wie folgt formuliert werden: 1 Mol entspricht die Menge einer Substanz, die als Strukturpartikel aus 12 g Kohlenstoff-12 enthielt.
Es wurde, daß 12 g dieses Isotops Atome enthaltene Menge gefunden auf die Avogadro-Konstante numerisch gleich ist.
Herkunft des Begriffs
Nur wenige verstehen, dass ein Maulwurf Chemie-Definitionen, die Geschichte dieses Konzept berücksichtigen. Wie allgemein der Begriff „Maulwurf“ verstanden wird, wurde von dem deutschen Chemiker Wilhelm Oswald eingeführt, der den Nobelpreis im Jahr 1909 gewonnen. Das Wort „Maulwurf“ leitet sich offensichtlich von dem Wort „Molekül“.

Interessant – die Avogadro-Hypothese, dass unter den gleichen Bedingungen in der gleichen Volumina verschiedener Gas, die die gleiche Menge der Substanz enthalten war, bevor Oswald nach vorne lange gesetzt, und die Konstante selbst wurde Avogadro im frühen XIX Jahrhundert berechnet. Das heißt, obwohl das Konzept der „Mole“, und es war nicht, die Idee von der Anzahl der Stoffe, die bereits war.
Grundformel

Die Menge der Substanz unterschiedlich ist, abhängig von den Daten des Problems. Diese Art ist die häufigste Formel, in der dieser Wert durch das Verhältnis des molaren Masse Gewicht ausgedrückt wird:
n = m / M
Es wird gesagt, dass die Menge der Materie – der Wert des Additivs. Das heißt, den Wert dieser Größe für das Gemisch zu berechnen, ist es notwendig, zunächst die Stoffmenge für jeden seiner Elemente und das Hinzufügen von ihnen zu bestimmen.
Eine andere Formel verwendet wird, wenn Menge der Teilchen bekannt ist:
n = N / N a
Wenn das Problem zeigt an, dass der Prozess unter normalen Bedingungen stattfindet, können Sie die folgende Regel verwenden: unter normalen Umständen nimmt jedes Gas der invariant Volumen – 22,4 Liter. Dann können Sie den folgenden Ausdruck verwenden:
nV / V m
Die Menge der Substanz wird durch Clapeyron Gleichung dargestellt:
n = pV / (RT)
Zu wissen, dass ein Maulwurf in der Chemie und Grundformel für die Anzahl der Mole des Stoffes zu bestimmen, ist es möglich, viele Probleme viel schneller zu lösen. Wenn Sie die Menge des Materials kennen, können Sie die Masse, Volumen, Dichte und andere Parameter.