Die Verwendung von Ethylen. Ethylen-Eigenschaften
Ethylen ist die einfachste von organischen Verbindungen wie Alkene bekannt. Dieses farblose brennbare Gas, einen süßen Geschmack und Geruch. Natürliche Quellen sind Erdgas und Öl, es ist auch ein natürliches Hormon , das in Pflanzen, in denen es um das Wachstum hemmt und fördert die Reifung der Frucht. Die Verwendung von Ethylen ist in der industriellen organischen Chemie üblich. Es wird durch Erhitzen von Erdgas, mit einem Schmelzpunkt von 169,4 ° C, Siedepunkt hergestellt – 103 ° C 9
Ethylen: strukturelle Merkmale und Eigenschaften
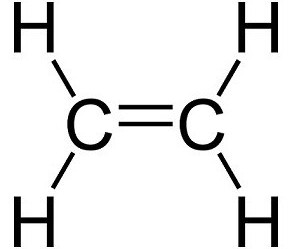
Kohlenwasserstoffe sind Moleküle, Wasserstoff und Kohlenstoff enthält. Sie variieren stark in Bezug auf die Anzahl von Einfach- und Doppelbindungen und strukturelle Ausrichtung der einzelnen Komponenten. Eine der einfachsten, aber biologisch und wirtschaftlich vorteilhafte Kohlenwasserstoff Ethylen ist. Es kommt in einer gasförmigen Form, es ist farblos und leicht entzündlich. Es besteht aus zwei doppelt gebundenen Kohlenstoffatom mit Wasserstoffatomen. Die chemische Formel ist C 2 H 4. Die strukturelle Form des Moleküls ist linear aufgrund der Anwesenheit einer Doppelbindung in der Mitte.
Ethylen ist süß Moschusgeruch, das macht es leicht, die Substanz in der Luft zu identifizieren. Dies gilt für Gas in reiner Form: Geruch verschwinden, wenn sie mit anderen Chemikalien gemischt werden.
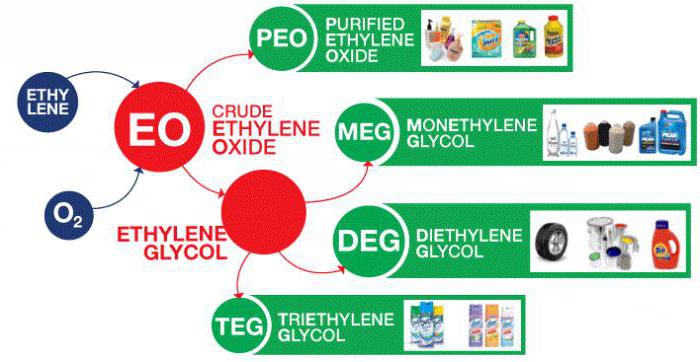
Scheme Ethylen-Anwendungen
das Monomer, aus dem großen Kohlenstoffketten aufgebaut sind, und als Ausgangsmaterial für weitere zwei-Kohlenstoff-Verbindungen: Ethylen wird in zwei Grundkategorien verwendet. Polymerisation – Wiederholen dieses eine Mehrzahl von Ethylen kleine Moleküle in größere kombiniert. Dieser Prozess findet bei hohen Drücken und Temperaturen. Anwendungen sind zahlreiche Ethylen. Polyethylene – ein Polymer, das vor allem in der Massenproduktion von Verpackungsfolien verwendet wird, Drahtbeschichtungen und Kunststoffflaschen. Eine weitere Verwendung von Ethylen als Monomer bezieht sich auf die Bildung von linearen α-Olefinen. Ethylen ist das Ausgangsmaterial für die Herstellung einer Reihe von zwei-Kohlenstoff – Verbindungen, wie Ethanol (Industriealkohol), Ethylenoxid (Frostschutzmitteln, Polyesterfasern und Folien) Acetaldehyd und Vinylchlorid. Zusätzlich zu diesen Verbindungen, Ethylen und Benzol Ethylbenzol Form, die bei der Herstellung von Kunststoffen verwendet wird , und synthetischen Kautschuk. Der betreffende Stoff ist eine der einfachsten Kohlenwasserstoffe. Allerdings Ethylen Eigenschaften machen es wirtschaftlich und biologisch bedeutsam.
kommerzielle Nutzung
Ethylen-Eigenschaften bieten eine gute Grundlage für eine kommerzielle große Menge an organischen (Kohlenstoff und Wasserstoff enthält) Material. Einzelethylenmoleküle können zusammen Polyethylen herzustellen verbunden werden (was eine Menge von Molekülen aus Ethylen bedeutet). Polyethylen wird Altkunststoffe zu machen. Darüber hinaus kann es für die Herstellung von Waschmitteln verwendet werden, und synthetische Schmierstoffe, die Chemikalien, die verwendet werden, die Reibung zu reduzieren. Die Verwendung von Ethylen für Styrole wichtig bei der Schaffung von Gummi und Schutzverpackung. Darüber hinaus ist es in der Schuhindustrie, vor allem Sportschuh, sowie bei der Herstellung von Autoreifen verwendet. Die Verwendung von Ethylen ist kommerziell wichtig, und das Gas selbst ist eines der am häufigsten produzierten Kohlenwasserstoffe global.
Gesundheitsgefahren
Ethylen ist ein Gesundheitsrisiko in erster Linie, weil es sehr leicht entflammbar und explosiv ist. Es kann auch als Medikament bei niedrigeren Konzentrationen wirkt, was zu Übelkeit, Schwindel, Kopfschmerzen und Verlust der Koordination der Bewegungen. Bei höheren Konzentrationen wirkt es als Anästhetikum, was zu Bewusstlosigkeit, Schmerzunempfindlichkeit und andere Reize. All diese negativen Aspekte können ein Grund zur Besorgnis sein, besonders für Menschen, die direkt mit Gas arbeiten. Die Menge an Ethylen, mit denen die meisten Menschen in ihrem täglichen Leben konfrontiert sind, sind in der Regel relativ klein.
Die Reaktion von Ethylen
1) Oxidation. Diese Zugabe von Sauerstoff, beispielsweise bei der Oxidation von Ethylen zu Ethylenoxid. Es wird bei der Herstellung von Ethylenglykol (1,2-Ethandiol) verwendet, die als Frostschutzmittel und bei der Herstellung von Polyester durch Kondensationspolymerisation verwendet wird.
2) Die Halogenierung – Umsetzung mit Ethylen Fluor, Chlor, Brom, Jod.
3) Die Chlorierung von Ethylen 1,2-Dichlorethan und die anschließende Umwandlung von 1,2-Dichlorethan in Vinylchlorid-Monomer zu bilden. 1,2-Dichlorethan ist ein nützliches organisches Lösungsmittel und ist eine wertvolle Vorstufe bei der Synthese von Vinylchlorid.  4) Die Alkylierung von – Kohlenwasserstoffe an der Doppelbindung, beispielsweise die Synthese von Ethylbenzol aus Ethylen und Benzol, gefolgt von der Umwandlung zu Styrol hinzugefügt wird. Ethylbenzol ist ein Zwischenprodukt für die Herstellung von Styrol, einem der am häufigsten verwendeten Vinylmonomere. Styrol – Monomer zur Herstellung von Polystyrol verwendet.
4) Die Alkylierung von – Kohlenwasserstoffe an der Doppelbindung, beispielsweise die Synthese von Ethylbenzol aus Ethylen und Benzol, gefolgt von der Umwandlung zu Styrol hinzugefügt wird. Ethylbenzol ist ein Zwischenprodukt für die Herstellung von Styrol, einem der am häufigsten verwendeten Vinylmonomere. Styrol – Monomer zur Herstellung von Polystyrol verwendet.
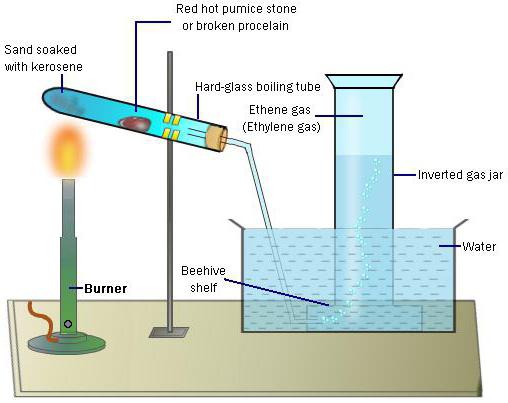
5) Bei der Verbrennung von Ethylen. Das Gas, das durch Erhitzen Ethylalkohol und konzentrierter Schwefelsäure erhalten.
6) Hydratation – die Reaktion mit der Zugabe von Wasser an die Doppelbindung. Die wichtigste industrielle Anwendung dieser Reaktion ist die Umwandlung von Ethylen zu Ethanol.
Ethylen und Verbrennung
Ethylen – ein Gas, ohne Farbe, die in Wasser schlecht löslich ist. Verbrennung von Ethylen in der Luft durch die Bildung von Kohlendioxid und Wasser begleitet. In reiner Form Gas Licht brennt Diffusionsflamme. Gemischt mit einer kleinen Menge an Luft, liefert sie die Flamme, die aus drei separaten Schichten bestehen, – der innere Kern – die unverbrannte Gas, blaugrüne Schicht und den äußeren Membran, wobei das teilweise oxidierte Produkt der vorgemischten Schicht in einer Diffusionsflamme verbrannt. Die sich ergebende Flamme zeigt eine komplexe Reihe von Reaktionen, und wenn die Gasmischung mehr Luftdiffusionsschicht verschwindet allmählich zugegeben wird.
Nützliche Fakten
1) Ethylen ist ein Pflanzenhormon natürlichen, es beeinflusst das Wachstum, Entwicklung, Reifung und Alterung von Pflanzen.
2) Gas ist nicht schädlich und nicht giftig für die Menschen bei einer bestimmten Konzentration (100-150 mg).
3) Es ist in der Medizin als Analgetikum eingesetzt.
4) Wirkung von Ethylen verlangsamt bei niedrigeren Temperaturen.
5) Ein charakteristisches Merkmal ist eine gute Penetration durch den meisten Substanzen, beispielsweise durch die Verpackungspappschachtel, Holz und sogar Betonwände.
6) Während es von unschätzbarem Wert für seine Fähigkeit ist, den Prozess der Reifung zu initiieren, kann es auch sehr schädlich sein, viele Früchte, Gemüse, Blumen und Pflanzen, den Alterungsprozess zu beschleunigen und die Verringerung die Qualität des Produkts und seine Haltbarkeit. Der Grad der Schädigung hängt von der Konzentration, Expositionsdauer und Temperatur.
7) Ethylen explosive bei hohen Konzentrationen.
8) Ethylen wird in der Glasindustrie für spezielle Zwecke für die Automobilindustrie eingesetzt.
9) Herstellung von Metallstrukturen: Gas als Sauerstoff-Brenngas für Metallschneiden, Schweißen und Hochgeschwindigkeits thermische Spritzen verwendet.
10) Öl: Ethylen wird als Kühlmittel verwendet, insbesondere bei der Herstellung von verflüssigtem Erdgas.
11) Wie bereits erwähnt, Ethylen ist eine hochreaktive Substanz, Darüber hinaus ist es auch sehr leicht entflammbar ist. Aus Sicherheitsgründen ist es in der Regel durch spezielle getrennte Pipeline transportiert.
12) Eine der häufigsten Produkte direkt aus Ethylen hergestellt ist aus Kunststoff.