Die Reaktion von CaCl2, H2SO4
Einer der Stolpersteine in den ersten Schritten der chemischen Gesetze und die Grundlagen des Studiums ist es, chemische Reaktionen zu schreiben. Daher Fragen über die Interaktion von CaCl2, fand H2SO4 nicht regelmäßig und systematisch. Lassen Sie uns die wichtigsten „Problem“ Momente untersuchen.
Nehmen molekulare Gleichung
Wechselwirkung zwischen Calciumchlorid (Salz) und Schwefelsäure fließt durch den Austauschmechanismus.
 Kennzeichnend für diese Reaktion ist:
Kennzeichnend für diese Reaktion ist:
- zwei Anschlüsse an dem Einlass (Rohstoff);
- zwei Anschlüsse am Ausgang (Produkt);
- völlige Fehlen von einfachen Substanzen.
Austausch miteinander reaktiven Gruppen werden die Reaktanden modifiziert, und die Gleichung die Form:
CaCl2 + H2SO4 = CaSO4 + 2 HCl.
Wie zu sehen ist, zwei komplexe Substanz, formändernden Ionen eine sehr unterschiedlichen Verbindungen: ein neues Salz (CaSO4) und Salzsäure (HCl).
Fließen zu Ende
Antwort auf diese Frage kann einfach durch in molekularer Form zu CaCl2, H2SO4 Reaktionsgleichung zu schreiben. Die Art der Produkte und wird alles abhängen. Bis zum Ende des Prozesses ist im Fall der Bildung:
- lösliches Material (Schlamm);
- flüchtige Verbindung (Gas);
- malodissotsiiruschego Reagenz (Wasser, schwache Elektrolyten).
In Rücksicht auf CaCl 2, H2SO4 Fall unter Calciumsulfat-Reaktionsprodukte – schwerlösliche Verbindung fällt entsprechend der Tabelle.
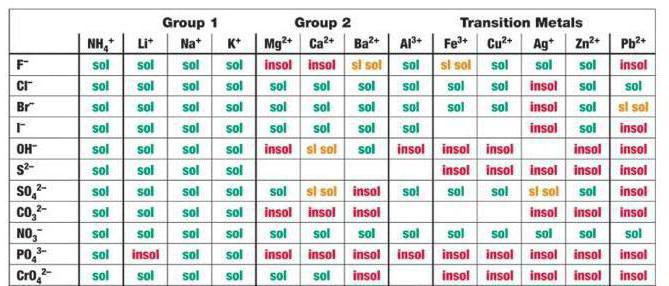
Folglich wird der Austauschprozess bis zum Ende gehalten werden.
Zusammengefasst ionische Form zwischen Aufzeichnungs CaCl 2, H2SO4
Schreiben Sie alle löslichen Verbindungen in Ionen und die Verringerung der reaktiven Gruppen wiederkehrende, so erhält man zwei Gleichungen das Unbekannte:
- vollständige ionische Form Aufzeichnung zwischen CaCl 2, H2SO4
Ca 2+ + 2 cl – + 2H + + so 4 2- = CaSO & sub4 ; + 2H + + 2 cl –
- eine verkürzte Form der Gleichung
Ca 2+ + SO 4 2- = CaSO4.
Es sei daran erinnert, daß nur Ionen löslicher Salze gemalt, Säuren, Basen (dies leicht aus speziellen Tabellen bestimmt wird). Schwache Elektrolyte Typ Kohlensäure oder Essigsäure in der molekularen Form immer geschrieben.
Jetzt wissen Sie, wie die Wechselwirkung zwischen Calciumchlorid (Salz) und Schwefelsäure.