Komplexverbindungen: Nomenklatur und Klassifikation
Die größte und vielseitigste unter den anorganischen Materialien ist eine Klasse von Komplexverbindungen. Um dies kann zu der Gruppe von organometallischen Verbindungen zugeschrieben werden, wie Chlorophyll und Hämoglobin. Es ist diese Verbindungen sind die Brücke, die die anorganische und organische Chemie in einer einheitlichen Wissenschaft verbindet. Unschätzbare Rolle in der Entwicklung von komplexen Materialien Kenntnissen auf dem Gebiet der analytischen Chemie und Kristallchemie, die Studie der wichtigsten biologischen Prozesse: Photosynthese, intern (zellulären) Atmung.
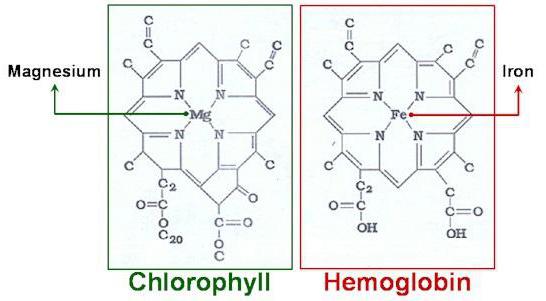
In diesem Artikel werden wir die Struktur und Nomenklatur der Komplexverbindungen, sowie die grundlegenden Prinzipien ihrer Klassifizierung untersuchen.
Koordination Theorie A. Werner
Am Ende des zwanzigsten Jahrhunderts Schweizer Wissenschaftler A. Werner bewiesen, dass das Molekül in jedem komplexen Substanz sind mehrere Strukturen, die bezeichnet worden sind jeweils das Zentralion, Liganden (Liganden) und der äußeren Koordinationssphäre. Dass wir klare Klassifizierung und Nomenklatur von komplexen Verbindungen waren, erklären wir diese Konzepte im Detail. Somit hat A. Werner wurde in Gegenwart von Ionen-Moleküle (in der Regel positiv geladen) erwiesen, die eine zentrale Position einnimmt. Er wurde als Komplexbildner, das Zentralion oder -atom bekannt. Es kann in der Nähe als neutrale Moleküle, die so genannte Liganden, und negativ geladene Anionen Partikel, die die inneren Koordinationssphäre des Materials bilden, angeordnet sein. Alle verbleibenden Partikel, die nicht in sie eingegeben wird, bilden die äußere Hülle des Moleküls.
So wird in Formel Cuprit Natrium Na 2 [Cu (OH) 4], ein zentrales Kupferatom in der Oxidationsstufe +2 und vier gidroksogrupp bilden die innere Kugel, während der Natriumionen in einiger Entfernung von dem Zentralatom in dem äußeren Bereich angeordnet sind.
Verfahren zur Bestimmung der Brenn Formeln und Namen von Substanzen
Bisher ist die Theorie von A. Werner die wichtigsten theoretischen Grundlagen für die komplexen Komplexe untersucht. Nomenklatur, dh die Namen dieser Stoffe durch die Regeln von der Internationalen Gesellschaft für Theoretische und Angewandte Chemie, erlassen hat.
Wir geben einige Beispiele von Formeln , von Substanzen, die das Platin – Komplexatom enthalten – K 2 [PtCl 6] oder Moleküle NH 3 – [Ag (NH 3) 2] Cl. Doppelaustauschreaktionen, molare Leitfähigkeit von Lösungen Röntgenbeugungsverfahren: Wie sich herausstellte, kann die Formel unter Verwendung der folgenden Methoden gewonnen werden. Betrachten Sie diese Methoden im Detail.
Da die Struktur von komplexen Platinverbindungen gezeigt
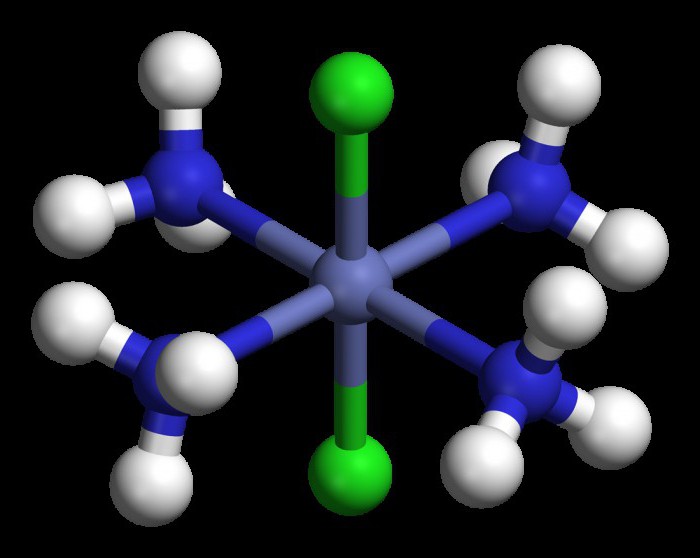
Substanzen dieser Gruppe sind durch das Vorhandensein im Molekül des Zentralplatinatom gekennzeichnet. Wenn die Verbindung PtCl 4 · 6NH 3 wirken Lösung von Silbernitrat, dann das gesamte Chlor in das Material mit dem Metall assoziiert Atomen und AgCl weiße Flocken gebildet. Dies bedeutet, dass alle Anionen Chlor in der äußeren Koordinationssphäre sind, während die Ammoniakmoleküle an die Zentralplatinatom gebunden wurden und mit diesem zusammen die innere Kugel ausgebildet ist.
Es bedeutet eine Koordinationsverbindung der Formel in dieser Form aufgezeichnet wird: [Pt (NH 3) 6] Cl 4 und Platin genannt Hexammin Chlorid. Durch die Verwendung von Röntgenstrahlbeugungsverfahren, die Chemiker erforscht und andere komplexe Verbindungen, die Nomenklatur werden im nächsten Abschnitt installiert werden.
Die kristallinen Verbindungen des Chroms
Die Struktur dieser Stoffgruppe wurde durch den physikalischen Prozess der Röntgenbeugung des darunterliegenden Röntgenbeugungsanalyse identifiziert. Die durch die Kristallgitter gestreut die elektromagnetische Welle durch die Wirkung von Elektronen, der Testsubstanz. Dies macht es sehr genau möglich, zu bestimmen, welche Gruppen von Atomen an Gitterplätzen sind. entsprechende Nomenklatur der Komplexverbindungen wurde auf Chrom enthaltenden Kristalle erzeugt. Beispiele von Namen isomere Hydrate von dreiwertigen Chromsalzen, gezogen durch Röntgenstrahlbeugungsverfahren, sind wie folgt: tetraakvadihlorohroma Chlorid (III), pentaakvahlorohroma Chlorid (III).
Es wurde festgestellt, dass Chromatom in diesen Materialien zu sechs verschiedenen Liganden gebunden. Wie kann die Geschwindigkeit bestimmen und jeder Faktor wirkt sich auf die Koordinationszahl?
Da das Zentralatom mit Liganden verknüpft
Um die oben aufgeworfenen Fragen zu beantworten, wie wir uns erinnern, dass in unmittelbarer Nähe des Komplexbildners sind mehrere Strukturen, die so genannte Liganden oder Liganden. Ihre Gesamtzahl und bestimmt die Koordinationszahl. Nach der Theorie von A. Werner, Empfang, Klassifizierung und Nomenklatur von komplexen Verbindungen sind auf diesem Indikatoren direkt abhängig. Es wird korrelativ mit der Oxidation des Zentralatoms verbunden. In den Verbindungen von Platin, Chrom, Eisen Koordinationszahl von höchstens gleich sechs; wenn das Komplexierungsmittel durch Atom von Kupfer oder Zink dargestellt ist – vier, wenn das Zentralatom Silber oder Kupfer – zwei.
Arten von Komplexverbindungen
In der Chemie unterscheiden als die wichtigsten Klassen und Reihen der Übergangs-Substanzen zwischen ihnen. Diskutiert in den vorhergehenden Zusammenfassungen komplexen Verbindungen, die Nomenklatur, die Anwesenheit in ihrer Struktur von Wassermolekülen angibt, sind aquacomplexes. Durch Ammin schließen Substanzen Ammoniak neutrale Teilchen enthalten, wie triiod triamminrody. Eigentümliche molekulare Struktur der Klasse von chelatbildenden Verbindungen. Ihr Name stammt aus dem biologischen Begriff chelicera – so Klaue decapod genannt. Diese Substanzen enthalten, Liganden, eine räumliche Konfiguration, die einen Komplexbildner enthält, wie Krallen. Solche Verbindungen schließen Eisen-III-Oxalat-Komplex, etilendiamminovy Platinkomplex mit der Oxidationsstufe +4, Aminoessigsäure-Salze, die Ionen von Rhodium, Platin oder Kupfer enthalten.

Regeln für die Erstellung der Namen von Komplexverbindungen
Die häufigste Testfrage bei der Suche nach Chemie im Laufe der High School ist: die komplexe Verbindung der IUPAC-Nomenklatur nennen. In einem speziellen Beispiel analysieren wir Algorithmus Titelsubstanz Kompilieren die folgende Formel: (NH 4) 2 [Pt (OH) 2 Cl 4].
- Name beginnt mit der Zusammensetzung des inneren Koordinationssphäre zu bestimmen. Es enthält Hydroxylgruppen sowie die Anionen von Chlor. Diese Titel fügen Sie die Endung -o. Wir erhalten digidrokso-, tetrahloro-.
- Jetzt finden wir den Komplexbildner seine Schreibweise lateinischen Namen, und fügen Sie dazu das Suffix -AT in Klammern ist der Grad der Oxidation zeigen: platinate (IV).
- Abgeschlossen mit innerer Kugel Symbol, nach außen bewegen. Wir nennen das Kation: in diesem Beispiel Ammoniumionen sind.
Als Ergebnis wird der Stoff einen Titel, in dem alle der oben genannten Struktur.
Die Verwendung von Komplexverbindungen
Zu Beginn dieses Artikels genannt werden die wichtigsten Vertreter der organometallischen Substanzen wie Hämoglobin, Chlorophyll, Vitamine. Sie spielen eine wichtige Rolle im Stoffwechsel. Komplexverbindungen in technologischen Zyklen von Schmelzen von Eisen- und Nichteisenmetallen eingesetzt. spezifische Komplexverbindungen, die Nomenklatur zeigen die Anwesenheit in ihren Molekülen von Kohlenmonoxid CO als Ligand – eine wichtige Rolle in der Metallurgie Carbonyle gespielt wird. Diese Verbindungen werden unter Erhitzen und reduzierten Metalle zerlegt, wie Nickel, Eisen, Kobalt aus ihren Erzen. Die meisten Komplexe werden auch als Katalysatoren bei der Herstellung Reaktionen Lacken, Farben und Kunststoffen verwendet.