Der Grad der Oxidation von Arsen: Arsen chemischen Eigenschaften
Bevor der Grad der Oxidation von Arsen unter Berücksichtigung seiner Position im Periodensystem und strukturelle Merkmale zu identifizieren. Außerdem rufen die grundlegenden physikalischen und chemischen Eigenschaften des chemischen Elements.

Die Situation in der SS
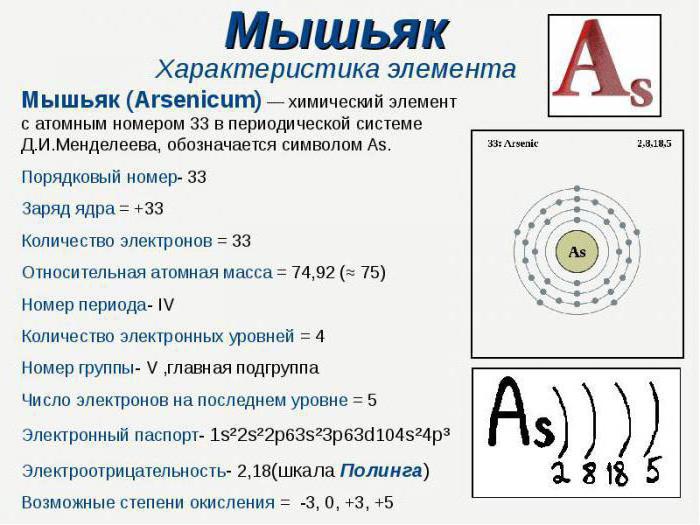
Grund Grad der Oxidation von Arsen, chemischen Eigenschaften, Anwendungen – all dies kann durch einen Blick auf dem Ort des Elements im Periodensystem. Arsen wird in der fünften Gruppe angeordnet, die Hauptuntergruppe ist eine repräsentative Familie von Stickstoff. Er hat eine relative Atommasse von 74,9216. Grund Arsen Oxidationsgrad mit der Gruppe verbunden ist, in dem sie in der MS gespeichert ist. Dieses Element 33 hat eine Seriennummer. Die Anzahl von Energieniveaus, die der Anzahl der Periode entspricht, in der sich das Element befindet, ist es vier.
Betrachten sie die Anordnung der Elektronen in jeder Kernhülle. Auf dem ersten Energieniveau ist nur zwei gepaarte Elektronen, ein zweiter Schale – Partikel besetzen acht: 2s und 6p. Auf der dritten Ebene, unter ihnen, ist es zehn d-Elektronen angeordnet, dass nur 18 Teilchen. Externes Energieniveau ist ein 2s-Elektron und drei p-ungepaarten Elektron. Das ist die Anzahl der Valenzelektronen den möglichen Grad der Oxidation von Arsen bestimmt.
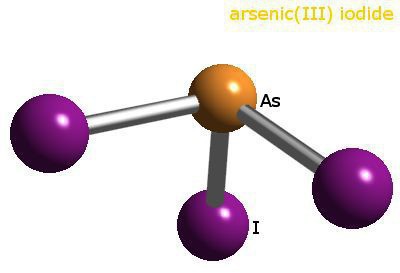
Seiten der Geschichte
Es Arsen bezieht sich auf fünf „alchemistischen“ Elemente, bekannt seit dem Mittelalter. Ein interessanter Punkt ist die Tatsache, dass vier von ihnen in der fünften Gruppe der SS sind. Damals konnte niemand den Grad der Oxidation von Arsen bestimmen, aber die Verbindung wurde erfolgreich für die Herstellung von Arzneimitteln verwendet, Farben zu schaffen.
Nach dem Wechsel von der Steinzeit bis in die Bronzezeit, lernten die Menschen diese Legierung mit speziellen Eigenschaften zu erzeugen. Es stellt sich heraus, dass es bis zu 7 Prozent des Arsens und 3 Prozent Zinn bestand. Wissenschaftler glauben, dass, wenn das erste Schmelzen von Bronze statt Malachit, grün Farbe, fälschlicherweise die grünen Kupfer-Arsen nahm Sulfidmineralien.
Die erstaunliche Leistung der resultierenden Legierung machte ihn bei den alten Meistern beliebt. Sie suchen speziell in der Natur Mineralien enthält die Substanz.
Grad von Arsenverbindungen in der Oxidation des Positiv-Typs, in Übereinstimmung mit seiner höheren Wertigkeit. Zur Identifizierung von Sulfiden, die Arsen, mineral erhitzt. Das Auftreten von spezifischem Knoblauchgeruch ist die Bestätigung der Anwesenheit in der Arsenverbindung. Nach und nach aus der Verhüttung von Bronze verweigert arsenous. Zu den Gründen für die Beendigung der Produktion von dem, was Wissenschaftlern der permanente Vergiftung des Meisters bei der Arbeit nennen.

natürliche Mineralien
In der Form des Mineralstoffen unter Berücksichtigung ist es aus der Antike bekannt. Zum Beispiel kann die Oxidationszahl von 3 in der Verbindung der Arsen Exponate bekannt in der alten China als „Stannaries dust“. Aristotle beschrieben Sandarak mineral darstellt Arsensulfid. Übersetzt aus dem Lateinischen seinen Namen wie „Goldfarbe“ klingt. Wir wenden es in jenen Tagen als gelber Farbstoff.
Im elften Jahrhundert Alchemisten werden drei verschiedene Arten von Substanzen. Der Grad der Oxidation von Arsen in den Verbindungen, die durch diese Arten dargestellt entspricht die Gruppennummer. Nennen Sie es weiß Arsen sechswertiges Oxid, Sulfid genannt gelb und rot – As4S4 (pararealgar).
Weiße Ausführungs Verunreinigungen bestand , wurde durch Sublimation in dem Brennverfahren erhalten von Kupfererzen, in denen die Zusammensetzung von Arsen enthalten. Da die Kondensation aus dem gasförmigen Zustand auftritt Ablagerung von Arsenoxid als weißen Plaque. Er hat seit der Antike als Mittel zur Schädlingsbekämpfung eingesetzt.
Im dreizehnten Jahrhundert wurde Albert der Große erhält metalloobraznoe Substanz. Er erhitzte mit Seife und gelben Arsen. Die Substanz, die durch die Wechselwirkung erhielt nicht anerkannt „mysteriöse Kommunikation“ sieben Planeten mit Metallen. Vielleicht ist dies aufgrund der Widersprüche durch die alten Alchemisten ergab Arsen „illegitimen“ Element betrachtet. Es war in diesen Tagen ist es die Fähigkeit, offenbart wurde Kupfer weiß zu verleihen, so wurde es als Mittel der bekannten „Venus Bleaching.“
Als einzelne Substanz hat das chemische Element nur in der Mitte des siebzehnten Jahrhunderts identifiziert worden. Deutsch Apotheker Johann Schroeder gelang es zu isolieren, die chemische Reduktion von Kohlenoxiden. Nach einiger Zeit gelang es Nikole Lemeri Metall Heizung Kaliseifen, Arsenoxid zu isolieren. Im 18. Jahrhundert ist dieses Metall wurde als ungewöhnlich „semi“ bekannt.
Im späten 18. Jahrhundert wurden schwedischer Chemiker K. V. Sheele erhalten Arsensäure, die den höchsten Grad der Oxidation von Arsen 5 manifestiert. Im neunzehnten Jahrhundert organische Substanzen, die Arsen enthalten, definiert.

in der Natur
Höhere und niedrigere Oxidationsgrad von Arsen eintreten in seiner natürlichen Verbindungen. In der Kruste prozentuale Konzentration eines gegebenen Elements nicht übersteigt 5 Gramm pro Tonne. In vielen Mineralien enthält es mit Nickel, Kobalt, Kupfer, Eisen zusammen.
Derzeit gibt es etwa zweihundert verschiedene natürliche Mineralien, die das chemische Element umfassen von uns betrachtet. In Anbetracht, dass sie den höchsten und den niedrigsten Grad der Oxidation des Arsens manifestieren, haben sie unterschiedliche Anwendung. Beispielsweise in Verbindung mit Antimon Arsen zeigt eine negative Oxidationsstufe. In Anbetracht die Tatsache, dass dieses Metall niedrige Elektronegativität ist, ein niedrigerer Oxidationsgrad von Arsen -3. Diese Figur ist typisch für Arsen-, sowie für Mineral allemontita.
Die meisten Verbindungen mit Metallen Arsen, die Spezifität der Zusammensetzung gegeben, ist eine intermetallische Verbindung, gekennzeichnet durch die Zusammensetzung des chemischen Elements variiert.
Eigenschaften Arsenid
Für Arsenid durch den Gehalt von mehreren Metallen mit ähnlicher Struktur der Kristallgitter gekennzeichnet ist. Diese Mineralien sind durch einen metallischen Glanz gekennzeichnet sind undurchsichtig, besitzen eine geringe Härte.
Als Beispiele für natürliche Arsenid können die folgenden Verbindungen prüfen:
- Löllingit ähnlich wie Pyrit;
- Nickelin rot Nickel Pyrit genannt;
- langisit;
- Oregon;
- Sperrylith.
Natürlich ist dies keine erschöpfende Liste solcher Mineralien – derzeit etwa fünfundzwanzig dieser Verbindungen emittieren. Zu den häufigsten in der Natur kann Arsenopyrit genannt Arsenkies genannt werden. Es ist ein Produkt, erhalten durch ein Schwefelatom in Pyrit Arsen ersetzt wird. Verbindungen eines solchen Plans, der nicht in dem höchsten Grad der Oxidation des Arsens gezeigt Sulfosalze genannt.
Ihre Kollegen glauben, Kobalt Glanz Gersdorffit, Enargit und Proust. Letzteres ist ein wichtiger Silbererzen, befindet sich in der oberen Schicht des Edel lebten. Die Struktur Sulfosalze können edle Metalle der Platingruppe. Unter ihnen Interesse irarsite und orsit. Ihre Zusammensetzung ist seltene Metalle verwendet, wie hervorragende Katalysatoren in der organischen und anorganischen Synthese.
Der maximale Grad der Oxidation des Arsens in seinen natürlichen Sulfiden gezeigt. Zum Beispiel repräsentiert die orangegelbe dimorph eine Arsensulfid (5). In den dreißiger Jahren des letzten Jahrhunderts, natürlichen Vorkommen von orpiment, auch in seiner Mitgliedschaft Sulfid, dreiwertigen Arsen, im Süden des Werchojansker Gebirge gefunden. Die Größe der erfaßten Kristalle betrug etwa 60 Zentimeter in der Länge und das Gewicht auf 30 kg geschätzt.

Eigenschaften Arsenate
Mögliche Oxidationsgrad von Arsen Salze können beispielsweise in Betracht gezogen werden. Arsensäure-Verbindungen bezeichnet Arsenat weisen somit die maximale Rate für das Metall: 5 beträgt. Als Beispiele für solche Verbindungen mit vorliegenden Erythrit eine leuchtend rosa Farbe. Das Salz bezeichnet Kobalt Farbe, es hat die Formel Co3 (AsO4) 2 * 8H 2 O. Es ist auch möglich Gasparo braunrot Farbtons als (Ce, La, Nd) ArO 4 zu beachten.
Im Zentrum von Schweden gefunden langbanovskie Ferromanganteilchen Karriere, wo es gefunden wurde und etwa fünfzig verschiedene Arsenate aus. Diese Verbindungen werden gebildet durch arsenige Säure mit Manganhydroxid reagieren, (2) bei niedrigeren Temperaturen.
Was erscheint Grad der Oxidation von Arsen zu Arsenat? Eigenschaften dieser Salze bestätigt das Vorhandensein von Schwefel in ihnen. Trotz des Fehlens von industriellen Anwendungen, deren ästhetisches Erscheinungsbild macht sie geeignet für minera Sammlungen zu schaffen.
Eine interessante Geschichte hat kupfernikel, die das Mineral Nichelino entspricht. Mittelalterliche deutsche Bergleute genannt Nickel auf den Berg des bösen Geistes, und „fake Kupfer“ genannt „kupfernikelem“. Meister wurde Ähnlichkeit kupferrotes Kristalle des Mineral Kupfererze enthüllt. Verwendet sie in Glas ein Produkt zu erhalten ist grün erhalten. Erst in dem Mineralogen Mitte des achtzehnten Jahrhunderts Axel Fredrik Cronstedt gelang aus dem Mineral Nickel zu isolieren.
Eigenschaften in der Natur
Arsen ist sehr inert, so kann es im nativen Zustand gefunden werden. Solcher Metallteil weist 2 bis 16 Prozent der Verunreinigungen, hauptsächlich Silber, Eisen, Kobalt sie sind, Nickel. In unserem Land wurde von den Geologen nativer Arsen in der Amur-Region, Transbaikalien entdeckt.
Es kann in Gesteinen und Mineralien, und in Pflanzen gefunden werden, so wird es zu Recht oft als allgegenwärtiges Element bezeichnet.
Was ist die maximale und der minimale Grad der Oxidation von Arsen? Der höchste Wert entspricht die Gruppennummer, wobei das aktive Element angeordnet ist, und ist +5. Es ist charakteristisch für die Verbindungen, bei denen es Eigenschaften aufweist, verringert wird. Lesen Sie mehr Verbindungen dieser einzigartigen Metall wird später in Betracht ziehen.
Der Globus Arsen sehr ungleich verteilt. Der Grund hierfür ist die Bildung der Lithosphäre und in der Sorption und Desorptionsprozesse auftretenden in Sedimenten und Böden.
Aufgrund der hervorragenden Löslichkeit des Metalls in Wasser wandert es leicht. Zum Beispiel in feuchtem Klima kommt es Auswaschung aus dem Boden, gefolgt von Bewegung zusammen mit dem Grundwasser, Flüssen.
physiologische Wirkung
Die wesentliche Menge von Arsen in Mineralwasser enthalten. Es gibt bestimmte Vorschriften über den Inhalt des Metalls. Wenn die zulässigen Werte übersteigt, gibt es eine ernste Gefährdung für den menschlichen Körper. Während der chemische Forschung wurde festgestellt, dass in natürlichem Wasser Arsen in verschiedenen Formen vorliegen kann. Was sollte der Grad der Oxidation von Arsen sein? Die Eigenschaften der Verbindungen, die in Wasser gefunden, das Vorhandensein von Metall in der Form von arsenous Säurelösung zu bestätigen.
Arsen in lebender Form enthält etwa 6 mg pro 1 kg. Ein Teil der Algen kann eine Substanz akkumulieren in einem solchen Ausmaß bezeichnet, dass es gefährlich für den menschlichen Körper sein kann. Einige der Arten in der asiatischen Ländern, sind in der Lage in einer reinen Säurelösung zu vermehren. Sie werden als Mittel der Kontrolle Ratten verwendet. In der menschlichen Hirngeweben, und eine ausreichende Menge des Metalls in seinen Muskeln. Darüber hinaus ist es in den Nagelplatten wird in den Haaren angesammelt.
physikalische Spezifikationen
Trotz der Tatsache, dass Arsen ein Metall ähnelt, hat es auch ein nicht-metallischen Zeichen. Zum Beispiel ist es Salze mit den Schwefelsäure zur Bildung wirkenden Ansäuern Element nicht in der Lage. Arsen kann in verschiedenen allotropen Modifikationen existieren unter Hinweis auf Phosphor. Die stabilste ist grau Arsen, die sublimiert, wenn in ähnlicher Weise Iod erhitzt.
Durch diese Änderung der elektrischen Leitfähigkeit schlechter als Kupfer, aber höher als Quecksilber. Bei Arsen Dämpfen Abkühlung kann weich transparent gelbe Farbe Substanz ähnlich den gelben Phosphor erhalten. Während des Erhitzens wird sie in eine andere allotrope Modifikation des chemischen Elements umgewandelt.
Wenn Arsen Dampfabscheidung auf Glas kann das Aussehen des Spiegelfilm beobachten. 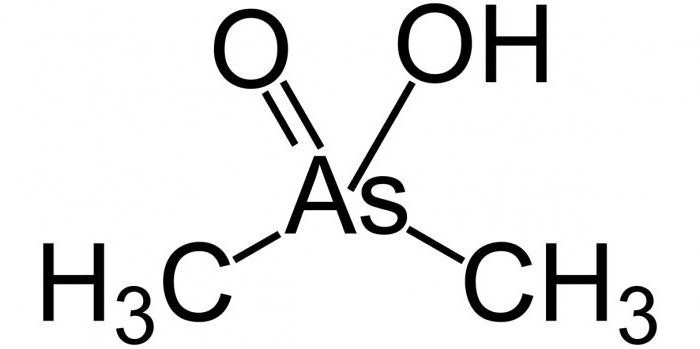
Arsenverbindungen
Der Grad der Oxidation des Arsens in der Top-Oxid-5, das mit seiner höheren Wertigkeits konsistent ist. Aber Sublimation von Metalldampf in feuchter Luft gebildeten schwarzen Film Arsen ihr Anhydrid As2O 3. Es ist in einer solchen Form im wesentlichen und Oxid des Elements vorhanden ist. Dieses Oxid weist amphoteren chemischen Eigenschaften.
Bei dem Oxidationsprozesse wird es umgewandelt ein höheres Oxid, die die Bedeutung der Arsens Oxidationsstufe +5 zeigt.
Das reine Metall wird mit verdünnter Salpetersäure oxidiert Säure H 3 AsO 3 zu ortomyshyakovistoy, wobei es mit einer Wertigkeit von 3 in ihrer chemischen Eigenschaften hat es sich um eine mittelstarke Säure analog Borsäure betrachtet wird. Salze betrachten Arsenit helle regenerierenden Eigenschaften aufweisen.
Das Metallchlorid hat den Oxidationszustand +3, als ein typisches Metallelement wirkt. Salzartige Arseniden, durch Reaktion mit aktiven Metallen zu unterziehen wässrige Hydrolyse gebildet. Beispielsweise Arsin (AsH 3) ist ein farbloses Gas toxisch, ohne Geruch.
Organometallverbindungen
Arsen kann verschiedene organometallische Verbindungen zu bilden. Zum Beispiel in dem späten 18. Jahrhundert destillative Oxid von Arsen (3) Kaliumacetat, erhielt Flüssigkeit rauchender einen unangenehmen Geruch. Das resultierende Produkt wurde genannt alarsinom. Nachfolgende Studien zeigten, dass in seinem Teil des Arsen vorhanden ist.
Im späten neunzehnten Jahrhundert, sind aromatische Arsine synthetisiert. Die Reaktion wurde unter der Einwirkung eines Gemisches aus Arsentrichlorid und einem Arylhalogenid mit metallischem Natrium durchgeführt wird. Einige dieser Produkte haben antimikrobiellen Eigenschaften unter Beweis gestellt. Bis heute ist die Synthese von Zehntausenden von Arsen organischer Substanzen.
Die Verwendung von Arsen
Mehr als die Hälfte des hergestellten Metalls wird in Form von verschiedenen Verbindungen verwendet. In seiner reinen Form ist es so gut wie nie verwendet. In kleinen Mengen ist es in die Lagerlegierungen eingeführt. Solche Zusätze haben eine positive Auswirkung auf die Härte des fertigen Produkts, so dass sie benötigt bei der Herstellung von elektrischen Kabeln und Batterien.
Die Mindestdosis des Arsens beitragen Korrosionsbeständigkeit zu verbessern, das thermischen Indikatoren, Messing und Kupfer zu verbessern. Wenn dieses Element keine zusätzliche Verunreinigungen enthält, in welchem Fall es wird bei der Herstellung von Halbleiterbauelementen umfasst. Schaffen sie, Arsen ist mit Germanium oder Silizium legiert.
Darüber hinaus ist er ein ausgezeichneter Dotierstoff Stahl zu schaffen. Als wertvolle Tipps Arsen Bedürfnisse und Nichteisenmetallurgie. Auch mit seinem niedrigen Gehalt in der Legierung kann stark die Festigkeit der hergestellten Produkte verbessern. Arsen erhöht die Fließfähigkeit beim Gießen von Kupfer, so dass es leichter, einen Draht zu erhalten.
Es gibt auch eine gewisse negativen Auswirkungen dieser Übergangsmetall-Produktion. Seine Anwesenheit im Erz Prozess verwandelt sich in eine gefährliche Industrie.
Unter den verschiedenen Arsenverbindungen von Interesse ist sein dreiwertiges Oxid. Er ist derzeit in der Glasindustrie verwendet wird. Salze mit der Angabe Nachfrage 5 als Antiseptika. Dieses Übergangselement ist eines des beliebtesten in der modernen chemischen Industrie, weil Exponate Dual Eigenschaften auf dem Prozessfluss des Mediums abhängig.















