Die physikalischen Eigenschaften der Essigsäure, die Formel
Gewöhnliche essbare Essig Flasche, die in der Küche jeder Hausfrau gefunden werden kann, hat viele andere Säuren und Vitamine zusammen. ein Paar Produkt fällt in das gekochte Essen Hinzufügen, Salate verursacht natürliche Geschmacksverbesserung. Aber nur wenige von uns dachten ernsthaft über die Eigenschaften und das tatsächliche Ausmaß der Nutzung der Hauptkomponente – Essigsäure.
Was ist das für ein Zeug?
Formel Essigsäure CH 3 COOH , die es auf die Anzahl der Carbonfettsäuren bezieht. Die Anwesenheit einer Carboxylgruppe (COOH) weist sie eine einbasische Säure. Die Substanz auf der Erde in einer organischen befundenen und synthetisch im Labor erhalten. Säure ist die einfachste, aber nicht weniger wichtige Vertreter seines Bereichs. Leicht löslich in Wasser, hygroskopisch.
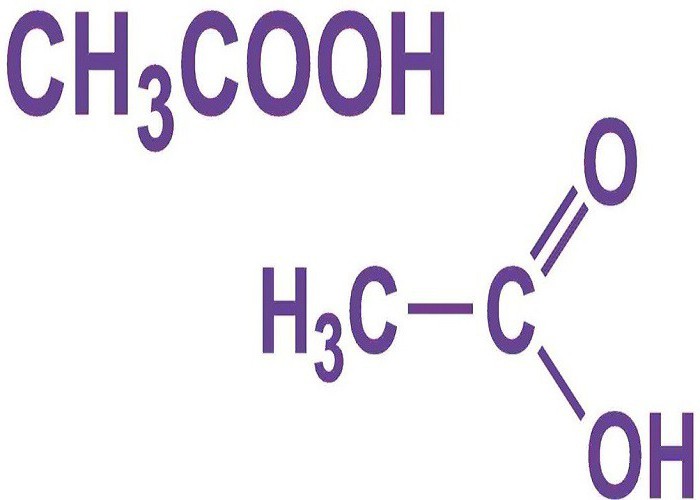
Die physikalischen Eigenschaften von Essigsäure und Dichte variieren mit der Temperatur. Bei Raumtemperatur beträgt 20 ° C Säure in einem flüssigen Zustand, eine Dichte von 1,05 g / cm 3. Es hat einen spezifischen Geruch und sauren Geschmack. Eine Lösung des Stoffes ohne Zusätze härtet und wird Kristalle bei einer Temperatur unter 17 ° C. Das Verfahren beginnt bei einer Temperatur von über 117 ° C. Methyl – Gruppe (CH 3) essigsäure der Formel Essigsäure siedende wird durch Umsetzung der Alkohole mit Sauerstoff erhalten: Stoffe und alkoholische Gärung von Kohlenhydraten, Säuern Wein.
Ein wenig Geschichte
Eröffnung des Essigs war einer der ersten in einer Reihe von Säure und wurde in Stufen erfolgen. Zunächst begann Essigsäure durch Destillation arabischen Gelehrten des 8. Jahrhunderts zu extrahieren. im alten Rom jedoch eine Substanz, die aus sauren Wein abgeleitet wurde als Universal-Sauce verwendet. Der Name aus dem Griechischen bedeutet „sauer“. Im 17. Jahrhundert in Europa, Wissenschaftler konnten reine Substanz Substanz extrahieren. Zu dieser Zeit nahm sie die Formel und fand eine ungewöhnliche Fähigkeit – Essigsäure im Dampfzustand gezündet eine blaue Flamme.
Bis zum 19. Jahrhundert haben Wissenschaftler das Vorhandensein von Essigsäure in einer organischen Form nur gefunden – als Teil der Verbindungen und Salze von Estern. Im Rahmen der Pflanzen und ihre Früchte: Äpfel, Trauben. Bei Menschen und Tieren, Schweiß Ausscheidung, Galle. Im frühen 20. Jahrhundert, nach dem Zufall russische Wissenschaftler extrahierten Acetaldehyd aus der Reaktion von Acetylen mit Quecksilberoxid. Derzeit ist der Verbrauch Essigsäure so groß ist, daß seine primäre Extraktion erfolgt nur synthetisch in großem Maßstab.
Produktonsmethoden
Ob die Form der reinen Essigsäure oder das Vorhandensein von Verunreinigungen in der Lösung, Es hängt von der Extraktionsmethode. Nahrung wird Essigsäure biochemisch während Ethanolfermentation erhalten wird. In der Industrie sekretieren verschiedene Methoden Säureextraktion. Üblicherweise werden die Reaktionen durch hohe Temperaturen und Gegenwart von Katalysatoren begleitet:
- Methanol in der Reaktion mit Kohlenstoff (Carbonylierung).
- Sauerstoff-Oxidation von Erdölfraktionen.
- Pyrolyse von Holz.
- Sauerstoff-Oxidation von Acetaldehyd.

Industrielles Verfahren zum effektiven und wirtschaftlichen biochemischen. Aufgrund eines industriellen Prozess, die Menge der Produktion Essigsäure im 20. und 21. Jahrhundert bis zu dem 19. Jahrhundert zu mehr hundert Mal verglichen. Derzeit stellen die Essigsäure durch Carbonylierung von Methanol-Synthese mehr als 50% des erzeugten Volumens.
Die physikalischen Eigenschaften von Essigsäure und deren Einfluss auf den Indikator
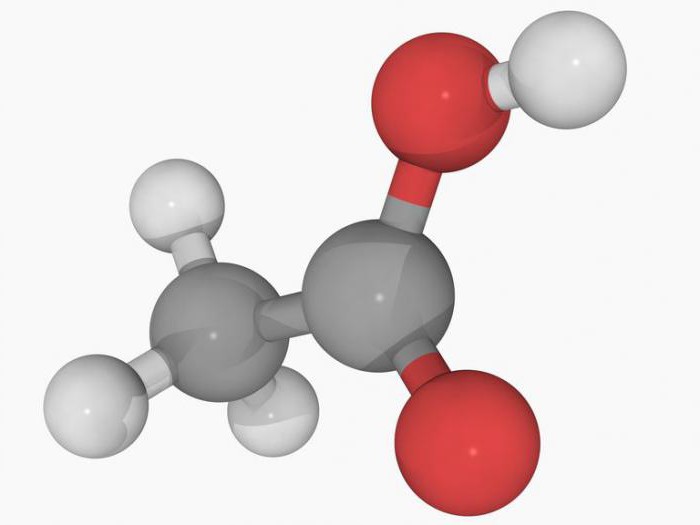
Die Essigsäure Flüssigkeit ist farblos. Acidität pH 2,4 wird durch Lackmuspapier leicht verifiziert. Essigsäure in Kontakt mit Lacken auf der Anzeige in rot. Die physikalischen Eigenschaften der Essigsäure visuell verändern. Wenn die Temperatur unter 16 ° C sinkt, nimmt die Substanz eine feste Form und ähnelt einem kleinen Eiskristallen. Es ist in Wasser leicht löslich und reagiert mit einer Vielzahl von anderen Lösungsmitteln als Schwefelwasserstoff. Essigsäure reduziert die Gesamtfluidvolumen bei der Verdünnung mit Wasser. beschreibt unabhängig die physikalischen Eigenschaften von Essigsäure, seine Farbe und Textur, die Sie im folgende Bild zu sehen.

Die Substanz wird bei einer Temperatur von 455 ° C unter Freisetzung von Wärme zu 876 kJ / mol gezündet. Das Molgewicht beträgt 60,05 g / mol. Die physikalischen Eigenschaften von Essigsäure als Elektrolyt in den Reaktionen sind schwach. Der Dielektrizitätskonstante 6.15 bei Raumtemperatur. Druck wie Dichte, – eine variable physikalische Eigenschaft Essigsäure. Bei einem Druck von 40 mm. Hg. Art. und eine Temperatur von 42 ° C , um den Kochvorgang zu beginnen. Aber schon bei einem Druck von 100 mm. Hg. Art. Sieden tritt nur bei 62 ° C
chemische Eigenschaften
Reagiert mit Metallen und Oxiden Substanz zeigt seine sauren Eigenschaften. Ausgezeichnete eine komplexere Verbindungen, Säureformen Salze aufzulösen, die Acetate :. Magnesium, Blei, Kalium usw. pK-Wert der Säure genannt werden, ist 4,75.
Während der Interaktion mit den Gasen kommen in Essig Substitutionsreaktion , gefolgt von der Verdrängung und bilden eine komplexere Säuren: Chlor, Iodessigsäure. Gelöst in Wasser, dissoziiert Säure mit der Freisetzung von Acetationen und Wasserstoffprotonen. Der Grad der Dissoziation beträgt 0,4 Prozent.
Physikalische und chemische Eigenschaften der Essigsäuremoleküle in der kristallinen Form Diamer Wasserstoffbrücken zu schaffen. Auch sind seine Eigenschaften notwendig komplexere Fettsäuren zu schaffen, die Biosynthese von Steroiden und Sterolen.
Labortest
Erkennen kann Essigsäure in Lösung durch Detektion seiner physikalischen Eigenschaften, wie Geruch erreicht werden. Genügend Lösung wurde zu einer starken Säure zugesetzt, die mit der Trennung von seinem Dampf Essig Salz zu verschieben beginnt. Durch Labordestillations COONa CH 3 und H 2 SO 4 möglich Essigsäure in trockenen Form zu erhalten.
Wir weisen Erfahrungen aus dem Schulunterricht in Chemie-Klasse 8. Die physikalischen Eigenschaften zeigen deutlich, Essigsäure rasstvoreniya chemische Reaktion. Es genügt, eine Substanz in Lösung, das Kupferoxid und leicht zu erwärmen, um es hinzuzufügen. Das Oxid wird vollständig gelöst, bläuliche Lösung.
Derivate Mittel
Qualitative Reaktionssubstanz mit vielen Lösungen bilden: Ester, Amide und Salze. Jedoch bei der Herstellung anderer Substanzen, sind die Anforderungen an den physikalischen Eigenschaften von Essigsäure hoch. Es muss immer einen hohen Grad an Auflösung hat und daher nicht über Fremd Verunreinigungen.
In Abhängigkeit von der Konzentration der wässrigen Lösung von Essigsäure eine Anzahl seiner Derivate zuzuordnen. Stoffkonzentration von mehr als 96% hat einen Namen – Eisessig. Essigsäure in 70-80% kann in Lebensmittelgeschäften gekauft werden, wo es genannt wird – Essigessenz. Vinegar hat eine Konzentration von 3-9%. 
Essigsäure und Alltag
Zusätzlich zu den Lebensmitteln Eigenschaften hat Essigsäure mehrere physikalische Eigenschaften, die die Menschheit ihre Anwendung im Leben gefunden hat. Eine Lösung mit einer niedrigen Konzentration der Substanz entfernt leicht Plaque von Metallgegenständen, Oberflächen Spiegel und Fenstern. Die Fähigkeit, Feuchtigkeit zu absorbieren, spielt auch profitieren. Essig ist ein gutes eliminiert muffige Gerüche in den Räumen, entfernt Flecken von Obst und Gemüse zu Kleidung.
Wie sich herausstellte , die physikalische Eigenschaft der Essigsäure – das Fett von der Oberfläche entfernen – können in der Volksmedizin und Kosmetologie verwendet werden. Eine schwache Lösung von Essig behandelt Haare, um sie glänzen zu machen. Die Substanz wird für die Behandlung von Erkältungen, die Entfernung von Warzen und Hautpilze weit verbreitet. An Dynamik gewinnt die Verwendung von Essig in der Zusammensetzung der kosmetischen hüllt Cellulite zu kämpfen.
Die Verwendung bei der Herstellung von
Die Salze der Verbindungen und andere komplexe Substanzen Essigsäure wirkt als unerlässliches Element:
- Pharmaindustrie. So erstellen: Aspirin, antiseptische und antibakterielle Salben, Phenacetin.
- Herstellung von synthetischen Fasern. Unbrennbaren Film, Celluloseacetat.
- LEBENSMITTELINDUSTRIE. Für eine erfolgreiche Konservierung, Herstellung Pickles und Saucen, als Lebensmittelzusatzstoff E260.
- Textilindustrie. Ausgestattet mit den Farbstoffen.
- Kosmetika und Körperpflegeprodukte-Industrie. Aromatische Öle, Cremes Hautton zu verbessern.
- Produktion Beizmittel. Verwendet als Insektizid und Beize von Unkraut.
- Herstellung von Lacken. Technische Lösungsmittel Aceton Produktion.

Jährlich Herstellung Essigsäure erhöht. Derzeit ist das Volumen in der Welt mehr als 400 Tausend Tonnen pro Monat. Säure wird von einem starken Stahltank transportiert. Lagerung in einem Kunststoffbehälter in vielen Branchen wegen der hohen physikalischen und chemischen Aktivität von Essigsäure ist auf einen Zeitraum von mehreren Monaten verboten oder eingeschränkt.
Sicherheit
Essigsäure mit hohen Konzentration einen dritten Grad der Zündung und giftige Gase. Es wird empfohlen, spezielle Masken und andere persönliche Schutzausrüstung zu tragen, wenn sie mit Säure zu arbeiten. Tödliche Dosis für einen menschlichen Körper von 20 ml. Zum Zeitpunkt der Freisetzung des Stoffes in die Säure verbrennt in erster Linie die Schleimhaut und wirkt sich dann andere Organe. In solchen Fällen brauchen sofortige Hospitalisierung.
Nach dem Kontakt mit der Säure in der exponierten Haut empfohlen sofort mit fließendem Wasser abgespült. Oberflächliche verbrühen Säure kann Gewebsnekrosen verursachen, die auch Hospitalisierung erfordert.
Interessante Fakten
Wissenschaftler Physiologie herausgefunden, dass eine Person nicht Empfang Essigsäure erforderlich ist – ohne Zusatzstoffe tun können. Aber die Menschen mit Unverträglichkeit gegenüber Säure, sowie Magenproblemen, Substanz kontra.

Essigsäure wird in der Typographie verwendet.
Substanz in einer geringen Menge wurde in Honig, Bananen und Weizen gefunden.
Nach dem Abkühlen Essigsäure und dramatisch mit shake it up Kapazität, können Sie ihre dramatische Verhärtung beobachten.
Eine geringe Konzentration von Essigsäure kann Schmerzsymptom von Insektenstichen und leichten Verbrennungen reduzieren.
Empfang in Lebensmitteln, die mit einem geringen Gehalt an Essigsäure reduziert den Cholesterinspiegel im Körper. Die Substanz ist stabilisiert auch den Blutzuckerspiegel bei Diabetikern.
Die Verwendung von Protein und Kohlenhydrat-Lebensmittel zusammen mit einer kleinen Menge Essigsäure erhöht ihren Verdaulichkeit Organismus.
Wenn das Essen zu salzig ist, nur ein paar Tropfen Essig Salzigkeit zu glätten.
endlich
Millennium Verwendung von Essigsäure führte zu der Tatsache, dass seine physikalischen und chemischen Eigenschaften finden ihren Weg an jeder Ecke. Hunderte von möglichen Reaktionen, Tausende von nützlichen Substanzen, durch die die Menschheit vor sich geht. Wichtig alle Funktionen von Essigsäure zu wissen, seine positiven und negativen Eigenschaften.
Vergessen Sie nicht, über die Vorteile, aber wir sollten immer daran denken, welcher Schaden einen sorglosen Umgang mit einer hohen Konzentration von Essigsäure verursachen kann. In seiner Gefahr, steht sie neben Salzsäure und Schwefelsäure. Immer Sicherheit erinnern, als Säure verwendet wird. Ordnungsgemäß und sorgfältig die Essenz von Wasser verdünnen.