Ksantoproteinovaya Reaktion auf Protein: Zeichen und Formel Gleichung
Um die qualitative Zusammensetzung vieler Lebensmittel ksantoproteinovaya Reaktion auf das Protein verwendet zu etablieren. Die Anwesenheit von aromatischen Aminosäuren in der Mischung wird in einer positiven Testprobe der Farbe ändern.
Was Protein
Es ist auch ein Protein genannt, die ein Baustoff für den lebenden Körper ist. Proteine pflegen Muskelmasse, zur Wiederherstellung der verletzten und tote Gewebestrukturen verschiedenen Organe, sei es Haare, Haut und Bänder. Mit ihrer Beteiligung produziert rote Blutkörperchen, durch den normalen Betrieb vieler Hormone und Zellen des Immunsystems bestimmt wird. 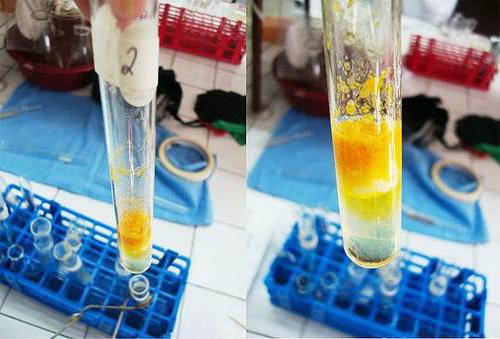
Dies ist ein komplexes Molekül , das ein Polypeptid ist , eine Masse von mehr als 6 ~ 10 3 Dalton. Proteinstruktur bildende Aminosäurereste in einer großen Anzahl von Peptidbindung gekoppelt.
Die Struktur von Proteinen
Das unterscheidende Merkmal dieser mit niedermolekularen Peptiden verglichenen Substanzen ist, dass sie eine dreidimensionale räumliche Struktur entwickelt, unterstützte Wirkungen mit unterschiedlichem Grad der Anziehung. Proteine besitzen vier Struktur. Für jede von ihnen hat seine eigenen Eigenschaften.
Als Grundlage der primären Organisation der Moleküle Aminosäuresequenz abgeleitet ist, die Struktur ksantoproteinovaya Reaktion auf das Protein erkennt. Diese Struktur ist eine sich periodisch wiederholende Peptidbindung -HN-CH-CO-, eine selektive Teil-Radikale die Seitenketten in Aminosäuren sind. Sie definieren weitere Eigenschaften des Stoffes als Ganzes.
Die primäre Proteinstruktur ist stark genug betrachtet wird, ist dies aufgrund der Anwesenheit von starken kovalenten Wechselwirkungen in der Peptidbindungen. Die Bildung von nachfolgenden Ebenen erfolgt in Abhängigkeit von den Attributen in der Anfangsstufe eingestellt.
Die Ausbildung der Sekundärstruktur ist möglich durch Verdrehen der Aminosäuresequenz wie in einer Spirale, in denen Wasserstoffbrückenbindungen zwischen den Windungen festgelegt werden.
Tertiärstufe Organisation von Molekülen durch die Anwendung eines von einer Spirale auf den anderen Fragmenten mit dem Auftreten aller möglichen Verbindungen zwischen ihnen, mit Wasserstoff, Disulfid, kovalente oder ionischer Verbindung gebildet. Das Ergebnis ist der Verein in Form von Kügelchen. 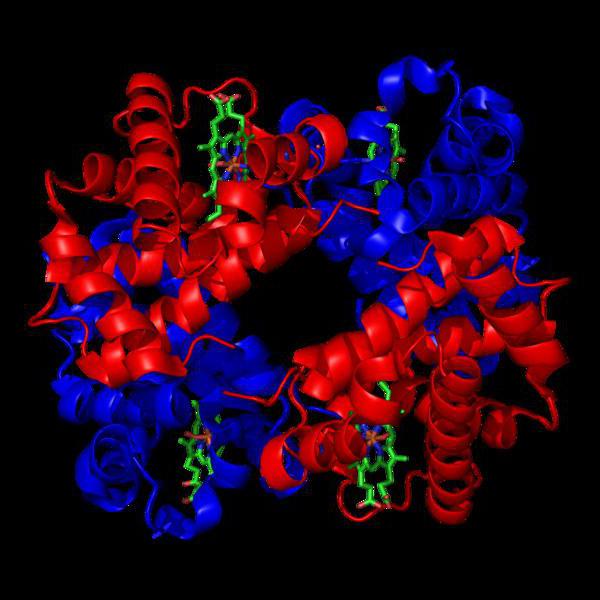
Die räumliche Anordnung der Tertiärstrukturen mit der Bildung von chemischen Bindungen zwischen ihnen führt zur Bildung der endgültigen Form des Moleküls oder quaternäres Ebenen.
Aminosäuren
Sie verursachen die chemischen Eigenschaften von Proteinen. Es gibt etwa 20 wichtigsten Aminosäuren, die die Polypeptide in einer anderen Reihenfolge bilden. Dies wird auch bezeichnet seltenen Aminocarbonsäure in Form Hydroxyprolin und Hydroxylysin gewonnenes basisches Peptid.
Als Zeichen der Erkennungs ksantoproteinovaya Proteinreaktion stellt die Gegenwart bestimmter Aminosäuren, die die Farbänderung von Reagenzien, um die Anwesenheit von spezifischen Strukturen, die in ihrer Zusammensetzung hindeutet.
Wie sich herausstellte, sind sie Carbonsäuren, die Substitution von Wasserstoffatom an der Aminogruppe aufgetreten sind.
Eine beispielhafte Struktur des Moleküls dazu dienen kann , eine Strukturformel Glycin (HNH- HCH- COOH) als die einfachste Aminosäure. 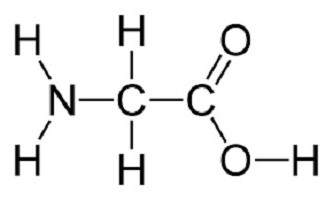
In diesem Fall ist einer der Wasserstoff CH 2 – durch einen Kohlenstoffrest mit mehr einen Benzolring, Amino, Sulfo, Carboxy ersetzt werden.
Was bedeutet ksantoproteinovaya Reaktion
Für die qualitative Analyse von Proteinen unter Verwendung verschiedener Techniken. Dazu gehören Reaktionen:
- Biuret mit dem Auftreten von violetter Farbe;
- Ninhydrin, um eine blau-violette Lösung zu bilden;
- Formaldehyd mit der Einrichtung einer roten Farbe;
- Nogier die grauschwarze Farbe auszufällen.
Bei der Durchführung erwiesen jede Methode die Anwesenheit von Proteinen und das Vorhandensein bestimmter funktioneller Gruppen in ihrem Molekül.
Es ksantoproteinovaya Reaktion auf das Protein. Es ist auch der Zusammenbruch Mulder genannt. Es bezieht sich auf die Farbreaktionen für Proteine, in denen es aromatische und heterocyclische Aminosäuren.
Ein Merkmal einer solchen Probe Prozess ist Nitrierung Salpetersäure cyclisches Aminosäurereste , insbesondere der Beitritt der Nitrogruppe an den Benzolring.
Das Ergebnis dieses Verfahrens ist die Bildung von Nitroverbindungen, die ausgefällt. Dies ist die grundlegende Funktion ksantoproteinovaya Reaktion.
Was die Aminosäure bestimmt
Verwendung einer derartigen Probe kann nicht alle Aminocarbonsäure nachgewiesen werden. Das Hauptmerkmal der ksantoproteinovaya Proteinnachweisreaktion – die Anwesenheit des Benzolrings oder heterocyclischen Rings im Molekül Aminosäuren.
Da das Protein von Aminocarbonsäuren zwei aromatischen isoliert, in dem es eine Phenyl-Gruppe ist (für Phenylalanin) und ein Hydroxyphenyl-Rest (in Tyrosin). 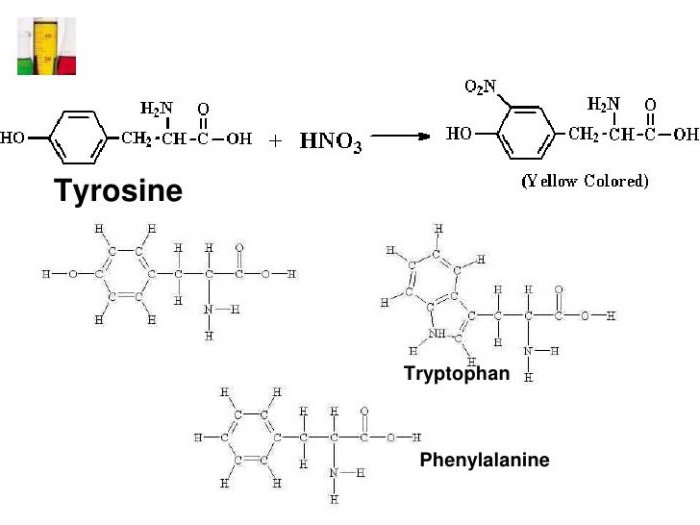
Mit ist ksantoproteinovaya Reaktions heterocyclische Aminosäure Tryptophan, Indol mit einem aromatischen Nukleus bestimmt. Das Vorhandensein der oben genannten Verbindungen in dem Protein gibt die charakteristische Farbänderung der Testumgebung.
Was Reagenzien
Für die Durchführung der Reaktion ksantoproteinovaya benötigen eine 1% ige Lösung von Eiprotein, oder pflanzlichen Ursprungs herzustellen.
Normalerweise verwendete Ei, die zur weiteren Trennung des Proteins aus dem Eigelb unterteilt ist. Für eine 1% ige Lösung von Protein wurde in einer zehnfachen Menge an gereinigtem Wasser verdünnt. Nach dem Auflösen der resultierenden Protein Flüssigkeit sollte durch mehrere Schichten von Seihtuch gefiltert werden. Diese Lösung sollte in einem kühlen Ort gelagert werden.
Es ist möglich, die Reaktion mit einem pflanzlichen Protein auszuführen. Zur Herstellung der Lösung Weizenmehl in einer Menge von 0,04 kg verwendet. 0,16 l gereinigtem Wasser. Die Bestandteile wurden in einem Kolben gemischt, die für 24 Stunden an einem kühlen Ort bei einer Temperatur von etwa + 1 ° C gebunden ist, Am Ende des Tages wurde die Lösung gerührt, gefolgt von Filtration davon zunächst mit einem Wattebausch und anschließend – ein Papierfaltenfilters. Die resultierende Flüssigkeit wurde in einem kühlen Ort aufbewahrt. Diese Lösung ist hauptsächlich in der Albuminfraktion.
Für die Reaktion ksantoproteinovaya als Haupt Reagenz verwendet Salpetersäure conc Durchführung. Weitere Reagenzien sind eine Lösung von 10% igem Natriumhydroxid oder Ammoniak, die Gelatinelösung und unkonzentrierten Phenol.
Die Methodik der
In einem sauberen Röhrchen ist 1% Proteinlösung -te Eier oder Mehl in einer Menge von 2 ml gebildet. Dazu wird etwa 9 Tropfen konzentrierter Salpetersäure zur Flockung gestoppt. Die resultierende Mischung wurde erhitzt, resultierende gelbe Niederschlag allmählich verschwindet und seine Farbe in Lösung geht. 
Wenn die Flüssigkeit entlang der Wand in dem Rohr abkühlt hinzugefügt etwa 9 Tropfen Natriumhydroxid, konzentriert, die für das Verfahren Überschuss vorhanden ist. Das Reaktionsmedium wird alkalisch. Inhalt wird orange Farbe im Reagenzglas.
Eigenschaften
Da ksantoproteinovaya qualitative Reaktion auf Salpetersäure durch die Wirkung der Proteine genannt, wird die Probe unter enthalten geführt fume hood. Beachten Sie alle Sicherheitsvorkehrungen, wenn mit konzentrierten ätzenden Substanzen arbeiten.
Die Freisetzung des Inhalts aus dem Rohr während des Erwärmungsprozesses auftreten, die berücksichtigt werden müssen, wenn es in einem Halter und Auswählen des Neigungs fixieren.
Dialing konzentrierter Salpetersäure und Ätznatron sollte nur unter Verwendung einer Glaspipette und Birnen Gummi verboten Pipette durch den Mund.
Relative Reaktion mit Phenol
Aus Gründen der Klarheit, zu verarbeiten und die Bestätigung der Anwesenheit der Phenylgruppen mit einer ähnlichen Probe Hydroxybenzol durchgeführt.
Das Rohr macht 2 ml verdünntem Phenol, dann nach und nach entlang der Wand, wurden 2 ml konzentrierte Salpetersäure zugesetzt. Die Lösung wurde zur Erwärmung unterzogen, wodurch es gelb wird. Diese Reaktion ist die Qualität der Gegenwart des Benzolrings. 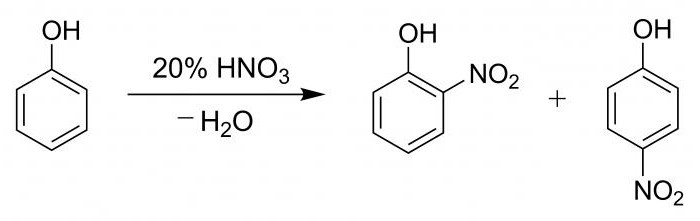
Prozess Hydroxybenzol mit Salpetersäure, gefolgt von der Bildung einer Mischung aus p-Nitrophenol und o-Nitrophenol in einem Anteil von 15 bis 35 nitriert.
Vergleichstest mit Gelatine
Um die ksantoproteinovaya Reaktion auf das Protein zeigt, zu beweisen eine Aminosäure mit aromatischer Struktur, Verwendung Proteinen, die keine phenolische Gruppe aufweisen.
In einem sauberen Röhrchen ist 1% igen Gelatinelösung in einer Menge von 2 ml gebildet. Dazu wird etwa 9 Tropfen konzentrierter Salpetersäure versetzt. Die sich ergebende Mischung wird erhitzt. Die Lösung wurde nicht in gelb gefärbt, die das Fehlen von Aminosäuren mit einer aromatischen Struktur beweist. Manchmal gibt es eine leichte Gelbfärbung der Umwelt aufgrund des Vorhandenseins von Proteinverunreinigungen.
chemische Gleichungen
In der zweistufigen Reaktion läuft ksantoproteinovaya Proteine. Formel erste Stufe Nitrierverfahren beschreibt Molekül Aminosäure mit konzentrierten Salpetersäure.
Ein Beispiel hierfür ist die Anbringung der Nitrogruppe zum Tyrosin-Nitrotyrosin und dinitrotirozina zu bilden. Im ersten Fall mit dem Benzolring einer NO 2 -Rest gebunden ist und die zweite Verbindung zwei Wasserstoffatome durch NO 2 ersetzt sind. Chemische Formeln ksantoproteinovaya Tyrosin-Reaktion durch Umsetzung mit Salpetersäure dargestellt Nitrotyrosin Molekül zu bilden.
Nitrierverfahren wird durch Übergang in farblose Färbung gelben Ton begleitet. Bei der Durchführung dieser Reaktion mit Proteinen die Aminosäurereste Phenylalanin oder Tryptophan, und die Farbe der Lösung ändert sich enthält.
Der zweite Schritt ist das Reaktionsprodukt der Nitrierung von Tyrosin-Molekülen, insbesondere Nitrotyrosin, mit Ammonium- oder Natriumhydroxid. Das Ergebnis ist ein Natrium- oder Ammoniumsalz, in der die gelb-orange Farbe. Eine solche Reaktion auf die Möglichkeit der Nitrotyrosin Moleküle bewegen sich in die chinoide Form zusammenhängt. Anschließend salz davon Nitronic Säure gebildet, das ein Chinon-System von konjugierten Doppelbindungen aufweist. 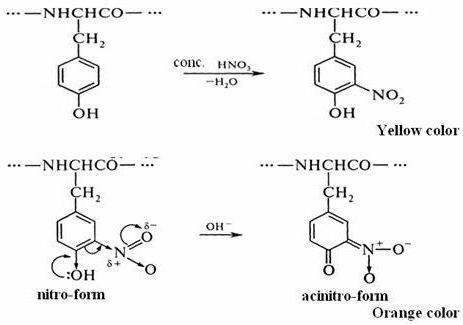
So endet ksantoproteinovaya Reaktion auf Proteine. Die Gleichung obigen zweiten Schritt dargestellt.
Ergebnisse
Während die Analyse von Flüssigkeiten in den drei Röhren enthalten ist, wird die Referenzlösung mit Phenol verdünnt. Substanzen mit einem Benzolring ergeben qualitative Reaktion mit Salpetersäure. Als Ergebnis ändert es Farbe der Lösung.
Wie bekannt ist, umfasst eine Gelatine hydrolysierter Form von Kollagen. Das Protein enthält nicht die aromatische Struktur der Aminosäuren. Keine Veränderung der Farbe des Mediums durch Umsetzung mit einer Säure.
Im dritten Teströhrchen gibt es eine positive Reaktion auf Proteine ksantoproteinovaya. Schlussfolgerung kann wie folgt gezeichnet werden: alle Proteine mit aromatischer Struktur, ob es sich um eine Phenylgruppe oder ein Indolring, die Änderung in der Farbe der Lösung gegeben werden. Dies ist aufgrund der Bildung von Nitroverbindungen mit einer gelben Farbe.
Durchführung einer Farbreaktion zeigt das Vorhandensein verschiedener chemischer Strukturen in Aminosäuren und Proteine. Beispiel Gelatine zeigt, dass seine Zusammensetzung Aminocarbonsäure umfasst eine Phenylgruppe oder eine cyclische Struktur nicht aufweisen.
Mit ksantoproteinovaya Reaktion kann durch Gelbfärbung der Haut erklärt werden, wenn es eine starke Salpetersäure angewandt. Die gleiche Farbe wird sich schaumige Milch während ihrer ähnlichen Analyse.
In der klinischen Laborpraxis wird diese Farbmuster nicht für den Nachweis von Eiweiß im Urin verwendet. Dies ist auf die gelbe Farbe des Urins selbst.
Ksantoproteinovaya Reaktion wurde zunehmend zur Quantifizierung von Aminosäuren, wie Tryptophan und Tyrosin, als Bestandteil verschiedenen Proteine verwendet.