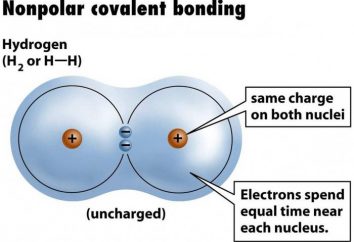
Die Hitze – es ist … Was ist die Wärmemenge, die während der Verbrennung freigesetzt?
Alle Substanzen eine innere Energie. Dieser Wert wird von einer Reihe von physikalischen und chemischen Eigenschaften charakterisiert, unter denen besondere Aufmerksamkeit sollte die Wärme bezahlt werden. Dieser Wert ist ein abstrakter mathematischer Wert, der die Stärke der molekularen Wechselwirkung Substanz beschreibt. Wärmeaustauschmechanismus zu verstehen , kann helfen , die Frage zu beantworten, welche Wärmemenge während der Abkühlung und Erwärmung Substanzen und deren Verbrennung freigesetzt wird .
Die Geschichte der Entdeckung von Wärme
Zu Beginn wird das Wärmeübertragungsphänomen beschrieben sehr einfach und klar: wenn die Temperatur des Materials ansteigt, wird es die Wärme, und im Fall der Abkühlung, es ordnet es in die Umwelt. Doch die Hitze – es ist nicht Bestandteil des Fluids oder der Körper betrachtet wurde vor drei Jahrhunderten gedacht. Man glaubte naiverweise, dass die Substanz besteht aus zwei Teilen: die Moleküle und Wärme. Nun wenige daran erinnern, dass der Begriff „Temperatur“ in Latein bedeutet eine „Mischung“, und zum Beispiel eine Bronze gesprochen als „Zinn und Kupfer Temperatur“.
Im 17. Jahrhundert gab es zwei Hypothesen, die eindeutig das Phänomen der Wärme und Wärmeübertragung erklären könnten. Zuerst im Jahr 1613, Galileo vorgeschlagen. Sein Wortlaut war: „Die Hitze – es ist eine ungewöhnliche Substanz, die in einen Körper und aus ihnen eindringen kann.“ Galileo diese Substanz Kalorien benannt. Er argumentierte, dass kalorische nicht verschwinden oder zerstört werden, und in der Lage nur von einem Körper zum anderen zu bewegen. Dementsprechend ist die in mehr kalorische Substanz, desto höher ist die Temperatur.
Die zweite Hypothese kam im Jahr 1620, und bot es den Philosophen Speck. Er wies darauf hin, dass unter den wuchtigen Schlägen des Hammers das Eisen erhitzt. Dieses Prinzip betrieben und das Feuer durch Reibung Betankung, führte Speck über die molekulare Natur der Wärme zu denken. Er behauptet, dass die mechanische Einwirkung auf den Körper seiner Moleküle beginnen, gegeneinander zu schlagen, um die Geschwindigkeit der Bewegung zu erhöhen und dadurch die Temperatur zu erhöhen.
Das Ergebnis war der Abschluss der zweiten Hypothese, die Wärme – das Ergebnis der mechanischen Einwirkung molekularen Substanzen miteinander. Diese Theorie für eine lange Zeit experimentell die Lomonosov zu rechtfertigen und zu beweisen versuchen. 
Die Hitze – es ist ein Maß für innere Energie,
Moderne Wissenschaftler haben zu folgendem Ergebnis gekommen: die thermische Energie ist das Ergebnis einer Wechselwirkung zwischen den Molekülen der Materie, dh .. Die inneren Energie des Körpers. Partikelgeschwindigkeit hängt von der Temperatur und der Wärmewert auf die Masse des Stoffes direkt proportional. Zum Beispiel hat ein Eimer Wasser eine höhere Wärmeenergie als der gefüllten Becher. Jedoch Untertasse mit heißer Flüssigkeit kann weniger Wärme als die kalten Becken.
Kalorische Theorie, die im 17. Jahrhundert vorgeschlagen wurde, Galileo, haben Wissenschaftler J. Joel und B. Rumford widerlegt. Sie bewiesen, dass die Hitze kein Gewicht hat und wird ausschließlich durch mechanische Bewegung der Moleküle charakterisiert.
Was ist die Wärmemenge, die während der Verbrennung des Stoffes freigesetzt? Spezifische Verbrennungswärme
Bis heute vielseitig und weit verbreitete Energiequellen sind Torf, Erdöl, Kohle, Erdgas oder Holz. Die Verbrennung dieser Stoffe wird eine bestimmte Wärmemenge zugewiesen wird zum Heizen verwendet, Mechanismen beginnen und dergleichen. D. Wie kann diesen Wert in der Praxis berechnen?
Für dieses Konzept eingeführte Verbrennung spezifische Wärme. Dieser Wert hängt von der Wärmemenge, die bei der Verbrennung von 1 kg einer bestimmten Substanz freigesetzt wird. Es wird mit dem Buchstaben q bezeichnet und ist in J / kg gemessen. einige der häufigsten Arten von Kraftstoff Nachfolgend finden Sie eine Tabelle mit Werten von q. 
Ingenieur die Konstruktion und Berechnung Motoren müssen die Menge der Wärme, die während der Verbrennung einer bestimmten Menge an Substanz freigesetzt kennen. Hierfür können wir indirekte Messungen durch die Formel Q = qm verwenden, wobei Q – der Heizwert der Substanz, q – spezifische Verbrennungswärme (Tabellenwert), und m – eine gegebene Masse.
Wärmebildung während der Verbrennung auf dem Phänomen der Energiefreisetzung bei der Bildung von chemischen Bindungen beruht. Das einfachste Beispiel ist die Verbrennung von Kohlenstoff, der in einen der verschiedenen Typen von modernen Brennstoffen enthalten ist. Kohlenstoff wird in der Gegenwart von Luft verbrannt, und verbindet sich mit Sauerstoff unter Bildung von Kohlendioxid. Die Bildung von chemischen Bindungen erfolgt unter Freisetzung von Wärmeenergie in der Umwelt, und die Energie der Person für ihre eigenen Zwecke nutzen angepasst.
Leider ist die unbedachten Ausgaben von wertvollen Ressourcen wie Öl oder Torf, führen können bald zur Erschöpfung der Quellen der Produktion dieser Kraftstoffe. Bereits heute gibt es elektrische Geräte und sogar neue Automodelle, die auf alternative Energiequellen wie Sonnenlicht basieren, Wasser oder Energie von der Erdkruste.
Wärmeübertragung
Die Fähigkeit , thermische Energie innerhalb des Körpers oder von einem Körper zum anderen auszutauschen wird die genannte Wärmeübertragung. Dieses Phänomen tritt spontan und tritt nur bei Temperaturdifferenzen. Im einfachsten Fall wird die thermische Energie von einer Erwärmung auf eine weniger erhitzten Körper übertragen, bis, bis ein Gleichgewicht hergestellt ist.
Körper wahlweise außerhalb des Wärmeübertragungsphänomen aufgetreten ist. In jedem Fall kann die Einstellung des Gleichgewichts auftritt und ein kurzer Abstand zwischen diesen Objekten, aber mit einer geringeren Geschwindigkeit, als wenn sie in Kontakt sind.
Die Wärmeübertragung kann in drei Typen unterteilt werden:
1. Wärmeleitfähigkeit auf.
2. Konvektion.
3. Der Strahlungsaustausch. 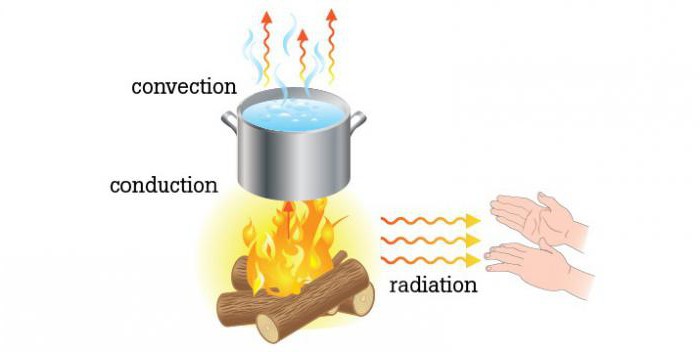
Wärmeleitfähigkeit
Dieses Phänomen beruht auf der Übertragung von Wärmeenergie zwischen den Atomen oder Molekülen der Materie. Übertragungsursache – zufällige Bewegung von Molekülen und deren ständige Kollision. Wodurch Wärme von einem Molekül zum anderen Kette übertragen. 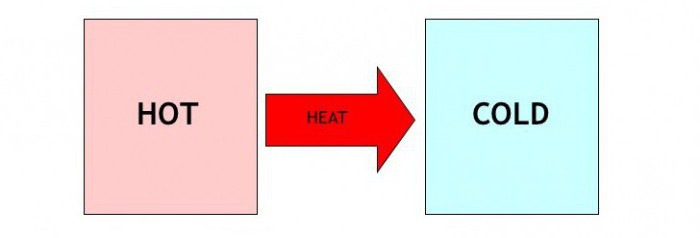
Wärmeleitungsphänomen beobachten kann aus jedem Eisenmaterial, wenn die Zündung Erythem Oberfläche glatt und erstreckt sich allmählich abschwächt (eine bestimmte Menge an Wärme in die Umwelt freigesetzt werden).
J. Fourier abgeleitet, eine Formel für Wärmefluß, der alle Mengen angesammelt hat, den Grad der Wärmeleitungsmaterial zu beeinflussen (siehe. Abbildung). 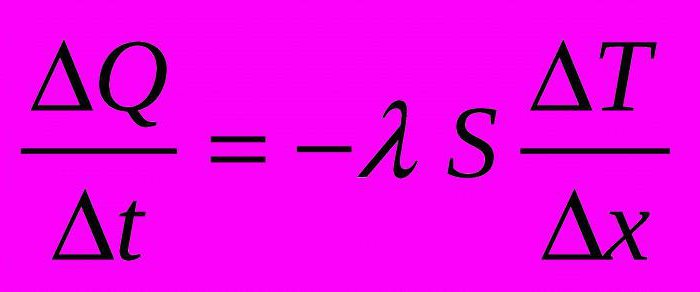
In dieser Formel steht Q / t – Wärmefluß, λ – Wärmeleitfähigkeitskoeffizient, S – Querschnittsfläche, T / X – das Verhältnis der Temperaturunterschied zwischen dem Körperende in einem gewissen Abstand befindet.
Wärmeleitfähigkeit ist der tabellierten Wert. Es hat praktischen Wert für die Isolierung eines Hauses oder Isolierung.
Strahlungswärme
Eine andere Möglichkeit, zu erwärmen, der auf dem Phänomen der elektromagnetischen Strahlung beruht. Sie unterscheidet sich von der Konvektion und der Wärmeleitung ist, dass die Energieübertragung in den Vakuumraum eintreten kann. Doch wie im ersten Fall, muss eine Temperaturdifferenz sein.
Radiant Austausch – ist ein Beispiel für die Übertragung von Wärmeenergie von der Sonne auf die Erdoberfläche, die vorzugsweise Infrarotstrahlung verantwortlich ist. Um zu bestimmen, wie viel Wärme der Erdoberfläche erreicht, wurden sie zahlreiche Stationen aufgebaut, die die Änderung des Indikators überwachen. 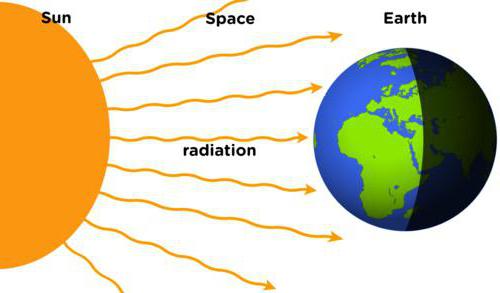
Konvektion
Konvektionsluft Strömungsbewegung ist direkt mit dem Wärmeübertragungsphänomen bezogen. Egal, wie viel Wärme wir eine Flüssigkeit oder ein Gas berichtet, gelösten Moleküle beginnen sich schneller zu bewegen. Aus diesem Grunde wird der Druck des gesamten Systems reduziert und die Menge an, im Gegenteil, zunimmt. Dies ist der Grund, warum die Bewegung von warmer Luft oder einem anderen Gas nach oben fließt.
Das einfachste Beispiel für die Verwendung des Phänomens der Konvektion in der Heimat Raumheizung kann über Batterien bezeichnet werden. Sie sind an der Unterseite des Raumes ist nicht nur so, und die Luft zu erwärmen, die steigen sollte, auf die Zirkulationsströmung durch den Raum führt. 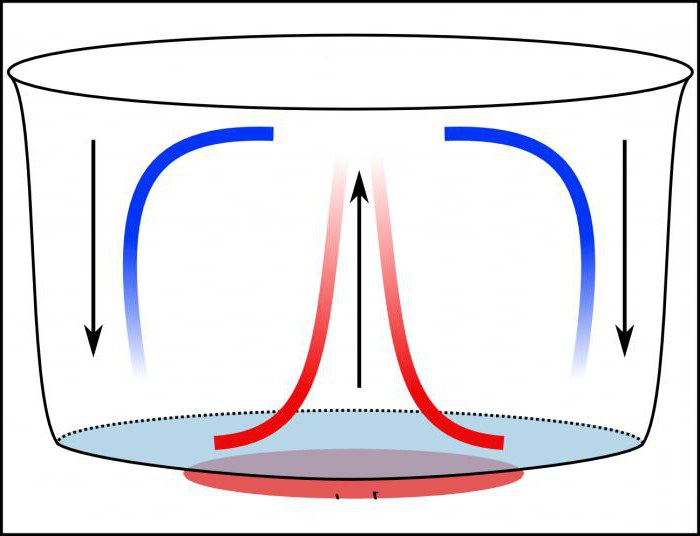
Wie kann man die Wärmemenge messen?
Die Wärme der Heizung oder Kühlung berechnet wird mathematisch eine spezielle Vorrichtung – Kalorimeter. Installieren von einem großen Gefß mit Wasser gefüllt ist, dargestellt isoliert. ein Thermometer für die anfängliche Temperatur des Mediums Messung wird in der Flüssigkeit abgesenkt. Dann tauchte in Wasser erwärmten Körper die Fluidtemperaturänderung nach der Einstellung des Gleichgewichts zu berechnen.
Durch Erhöhen oder das Medium abnehm t bestimmt wird, die Wärmemenge zum Erhitzen des Körpers aufgewendet werden. Das Kalorimeter ist ein einfaches Gerät, das die Temperaturänderung registrieren.
Auch kann ein Kalorimeter berechnen, wie viel von der Hitze bei der Verbrennung von Materialien freigesetzt. Zu diesem Zweck wird ein mit Wasser gefülltes Gefäß, stellte „die Bombe.“ Diese „Bombe“ ist ein geschlossene Behälter, in dem die Testsubstanz befindet. Um dies summierte spezielle Elektroden für die Zündung und die Kammer wird mit Sauerstoff gefüllt. Nach dem vollständigen Verbrennung Mitteln aufgezeichnet in Wassertemperatur zu ändern.
Während dieser Experimente festgestellt, dass die Wärmequellen sind chemische und Kernreaktionen. Kernreaktionen treten in den tieferen Schichten der Erde, die Hauptwärmeversorgung des gesamten Planeten zu bilden. Sie werden auch von Menschen zu erzeugen Energie bei der Fusion verwendet.
Beispiele für chemische Reaktionen werden Substanzen und die Zersetzung von Polymeren auf Monomere im menschlichen Verdauungssystem zu verbrennen. Die Qualität und Quantität der chemischen Bindungen im Molekül bestimmt, wie viel Wärme am Ende abheben.
Was wird durch die Wärme gemessen?
Die Einheit der Wärmemessung im SI-System ist die Joulesche (J). Auch Nicht-SI-Einheiten sind im Alltag – Kalorien. 1 Kalorie gleich 4,1868 J und dem internationalen Standard basierend auf 4184 J. Thermochemie. Frühere britische Wärmeeinheit BTU erfüllt, die von Wissenschaftlern selten benutzt hat. 1 BTU = 1,055 J.